Bevezetés a kovalens kötések világába
A kémia egyik legfontosabb témaköre a kovalens kötés, amely meghatározza, hogyan kapcsolódnak össze az atomok molekulákká. A kovalens kötések révén az atomok elektronokat osztanak meg egymással, így stabilabbá válik az elektronszerkezetük, és kialakulnak a mindennapjainkban is fontos molekulák.
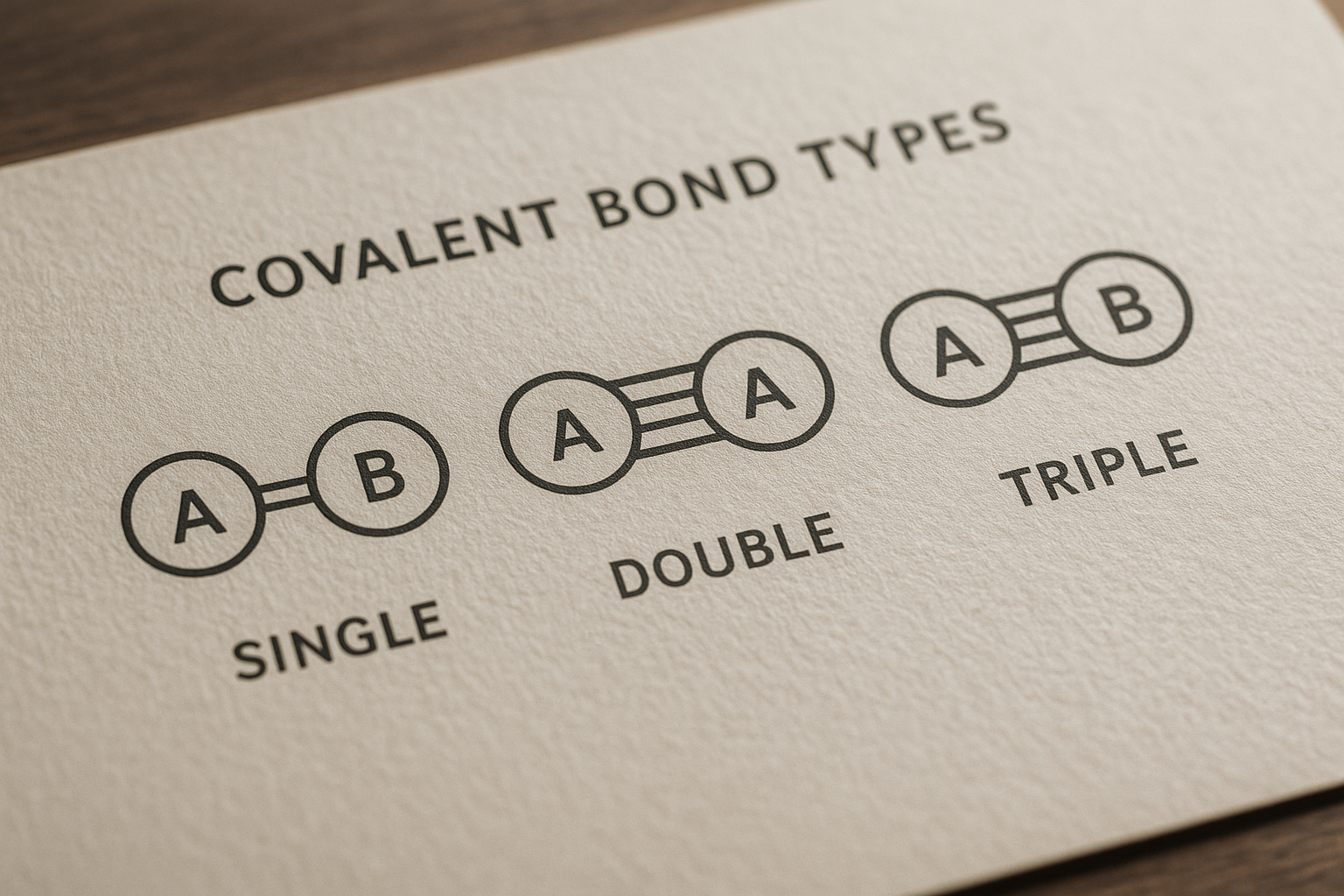
A kovalens kötések típusainak – az egyszeres, kettős és hármas kötéseknek – a megértése elengedhetetlen minden kémiával foglalkozó számára. Ezek a kötések határozzák meg, milyen tulajdonságai vannak egy anyagnak, legyen szó vízről, oxigénről vagy akár műanyagokról.
A kovalens kötések nemcsak a laboratóriumokban és tankönyvekben, hanem a mindennapi életünkben is jelen vannak: az ivóvíz, a levegő, a gyógyszerek, a műanyagok mind-mind kovalens kötéseket tartalmazó molekulákból épülnek fel. Megértésük nélkülözhetetlen a természet, a technológia és az orvostudomány világában egyaránt.
Tartalomjegyzék
- Mi is az a kovalens kötés és hogyan jön létre?
- Az egyszeres kovalens kötés szerkezete és példái
- Az egyszeres kötés fizikai és kémiai jellemzői
- Kettős kovalens kötés: kialakulás és sajátosságok
- Miben különbözik a kettős kötés az egyszerestől?
- A hármas kovalens kötés: szerkezet és jelentőség
- Hármas kötés előfordulása a mindennapi életben
- Kovalens kötések polaritása és hatásai
- Kötéshossz és kötéserősség az egyes típusoknál
- Kovalens kötés típusok összehasonlítása táblázatban
- Összegzés: a kovalens kötések szerepe a kémiában
Mi is az a kovalens kötés és hogyan jön létre?
A kovalens kötés egy olyan elsőrendű kémiai kötés, amely két atom között jön létre közös elektronpárok megosztásával. Ez a kötéstípus jellemzően nemfémek között alakul ki, ahol az atomok nem tudják teljes egészében átadni vagy felvenni az elektronokat, hanem közösen használják őket.
A kötés lényege, hogy a kapcsolódó atomok külső elektronhéján lévő elektronok közösen elfoglalt teret képeznek, amit kötő elektronpárnak hívunk. Egy egyszerű példával: a hidrogénmolekula (H₂) két hidrogénatomja egy-egy elektronját megosztja, így együtt egy stabilabb elektronpárt alkotnak.
A kovalens kötés tehát a molekulák alapvető építőköve, és meghatározza azok szerkezetét, tulajdonságait. Egyes molekulákban egyetlen, míg másokban több elektronpár is kialakíthat kovalens kötést, így jönnek létre az egyszeres, kettős vagy hármas kötések.
Az egyszeres kovalens kötés szerkezete és példái
Az egyszeres kovalens kötés a legegyszerűbb és leggyakoribb kötéstípus. Ilyenkor két atom egymással egyetlen elektronpárt oszt meg. Az ilyen kötés egyetlen vonallal jelölhető a molekulák szerkezeti képleteiben, például H–H vagy Cl–Cl.
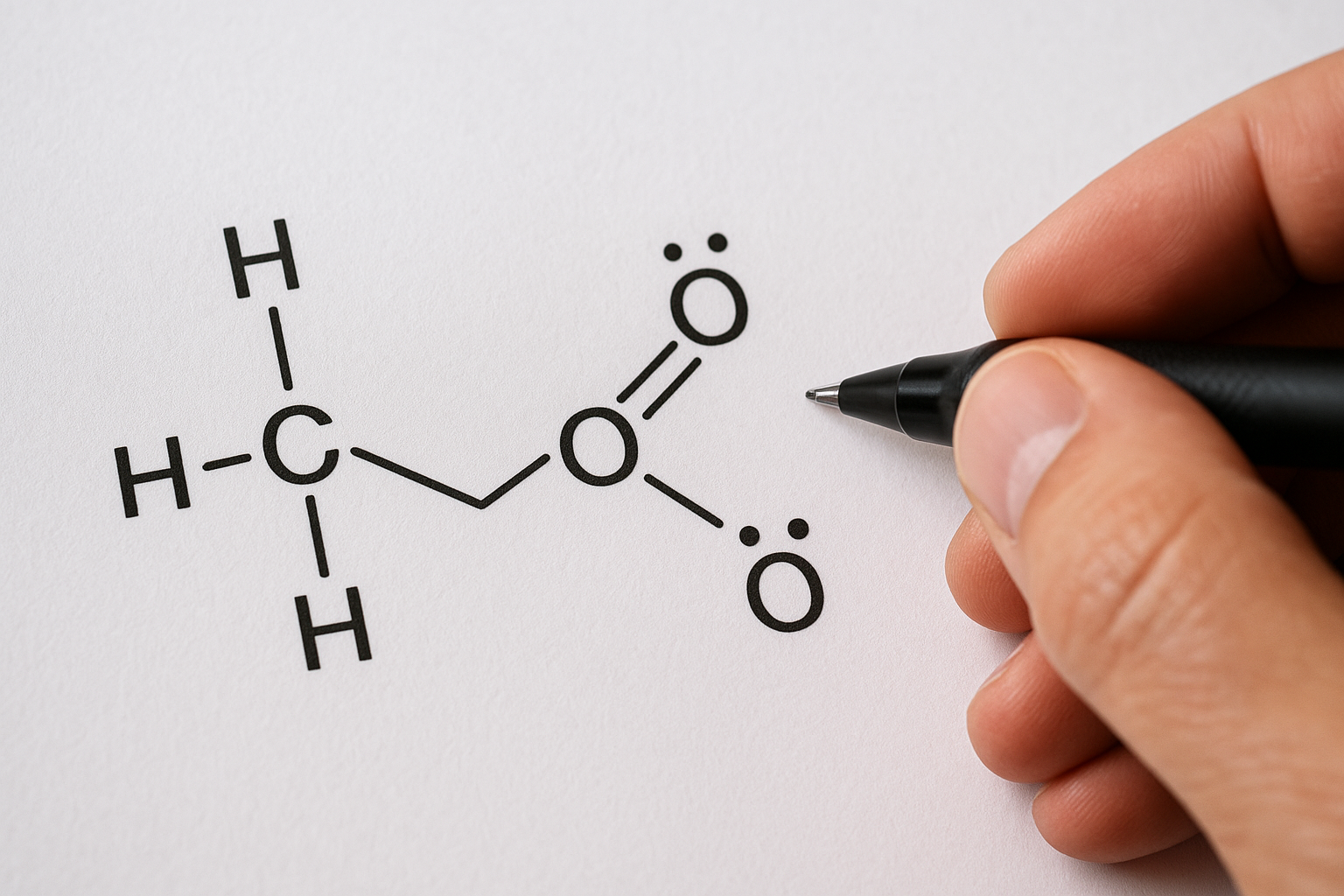
Egyszeres kötést találunk például a vízmolekulában (H₂O), ahol az oxigén atom két hidrogénatommal lép kapcsolatba, mindegyikkel egy-egy közös elektronpárt alkotva. Hasonlóképp, a metánmolekula (CH₄) négy egyszeres kovalens kötéssel kapcsolja össze a központi szénatomot a hidrogénatomokkal.
Az egyszeres kötés σ-kötés (szigma-kötés) típusú, ami azt jelenti, hogy az elektronpár a két atommag közötti térben helyezkedik el. Az egyszeres kötések általában nagyobb kötéshosszal és kisebb kötéserősséggel rendelkeznek, mint a többszörös kötések.
Ez a kötéstípus a mindennapi molekulákban rendkívül gyakori, például a hidrogén-kloridban (HCl), az ammóniában (NH₃) és számos szerves vegyületben is.
Az egyszeres kötés fizikai és kémiai jellemzői
Az egyszeres kovalens kötés jellemzői közé tartozik a stabilitás és a mérsékelt kötéserősség. Ezek a kötések általában kevéssé reaktívak, de bizonyos körülmények között (például magas hőmérsékleten vagy katalizátor jelenlétében) mégis bonthatóak.
Az egyszeres kötéssel rendelkező molekulák általában nagyobb mozgékonysággal bírnak, mivel a kötés körül az atomok szabadon elfordulhatnak (rotáció). Ez különösen fontos például a szénláncok rugalmasságában a szerves vegyületek esetén.
Az egyszeres kötések kötéshossza általában nagyobb, mint a kettős vagy hármas kötéseké, és kötési energiájuk alacsonyabb. Példaként a C–C kötés kötéshossza körülbelül 154 pm (pikometer), míg a C=C és C≡C kötések ennél rövidebbek.
A molekula polaritása is gyakran függ az egyszeres kötésben részt vevő atomok elektronegativitásától, például a H–Cl kötés erősen poláris, míg a H–H kötés apoláris.
Kettős kovalens kötés: kialakulás és sajátosságok
A kettős kovalens kötés akkor jön létre, ha két atom két-két elektronpárját osztja meg egymással. Ez azt jelenti, hogy összesen négy elektron vesz részt a kötés kialakításában, amely egy szigma- és egy π-kötésből (pi-kötésből) áll. Képlettel legtöbbször két vonallal: O=O vagy C=O.
Tipikus példa a szén-dioxid (CO₂) vagy az oxigénmolekula (O₂), ahol egy kettős kötés található. A szerves kémiában is gyakran találkozunk kettős kötéssel, például az etén (C₂H₄) molekulában.
A kettős kötés merevebb szerkezetet eredményez, nem engedi az atomok szabad elfordulását a kötés tengelye körül. Ennek köszönhető a geometriai izoméria, amely számos szerves vegyületben megfigyelhető.
A kettős kovalens kötés rövidebb és erősebb az egyszeres kötésnél, ami befolyásolja a molekulák reaktivitását és stabilitását is. A kettős kötések jellemzően reakcióképesebbek, például könnyen alávethetők addíciós reakcióknak.
Miben különbözik a kettős kötés az egyszerestől?
A legfontosabb különbség, hogy a kettős kötés két közös elektronpárból áll, míg az egyszeres kötés csak egyből. Ez a többszörös kötés nagyobb kötési energiát és rövidebb kötéshosszt eredményez.
A kettős kötés szerkezetében megtalálható egy σ-kötés (ami tengelyszimmetrikus) és egy π-kötés (ami a tengelyen kívüli térben helyezkedik el). A π-kötés jelenléte miatt a kettős kötés merev, az atomok nem tudnak szabadon elfordulni, ami jelentős kémiai és fizikai következményekkel jár.
A kettős kötés reaktivitása nagyobb, mivel a π-kötés könnyebben bontható, így például az alkének addíciós reakciókban vesznek részt. Az ilyen kötések a molekulák szerkezetének merevségét is növelik, ami fontos például a biológiai folyamatoknál.
A kettős kötés jelenléte a molekulák fizikai tulajdonságait is befolyásolja, például az olvadás- és forráspontot, polaritást, oldhatóságot.
A hármas kovalens kötés: szerkezet és jelentőség
A hármas kovalens kötés a legerősebb a három kötéstípus közül. Ilyenkor két atom három közös elektronpárt oszt meg egymással, vagyis összesen hat elektron vesz részt a kötés kialakításában. Ezt a kötéstípust három vonallal jelöljük: N≡N, C≡C.
A hármas kötés szerkezetileg egy σ-kötésből és két π-kötésből áll. A σ-kötés a két atommag között, a π-kötések pedig a tengely síkján kívül találhatók, ami tovább növeli a kötés erősségét és rövidségét.
A legismertebb példa a dinitrogén (N₂), ahol két nitrogénatom között hármas kovalens kötés található. Emellett az acetilén (C₂H₂), illetve néhány szerves molekula is tartalmaz ilyen kötést.
A hármas kötés nagyon rövid és nagyon erős, ami miatt ezek a molekulák kevésbé hajlamosak reakcióba lépni, viszont ha mégis, akkor sok energia szabadul fel a kötés felbontásakor.
Hármas kötés előfordulása a mindennapi életben
A hármas kovalens kötés nemcsak a tankönyvekben, hanem a mindennapi életünkben is jelen van. A levegő nitrogéntartalma (N₂) a Föld légkörének mintegy 78%-át alkotja, és ebben a molekulában hármas kötés található.
Az acetilén (etinszármazék, C₂H₂) például a hegesztéstechnikában használt éghető gáz. A hármas kötés miatt az acetilén energiatartalma igen magas, oxigénnel elégve nagyon magas hőmérsékletet produkál.
A hármas kötés jelenléte a molekulában stabilitást és gyakran inert (tehetetlen) tulajdonságokat is ad. Ezért például az atmoszferikus nitrogén gáz biológiailag csak speciális körülmények között, például villámlás vagy nitrogénkötő baktériumok segítségével reagál más anyagokkal.
A szerves kémiában a hármas kötések fontos szerepet játszanak például a műanyagok, gyógyszerek előállításában is, mivel egyedi reakcióképességgel bírnak.
Kovalens kötések polaritása és hatásai
A kovalens kötés lehet poláris vagy apoláris, attól függően, hogy a kötésben részt vevő atomok elektronegativitása mennyire különbözik egymástól. Apoláris kovalens kötés akkor alakul ki, ha két azonos vagy majdnem azonos elektronegativitású atom között jön létre, például H₂, O₂, N₂ molekulákban.
Poláris kovalens kötés viszont eltérő elektronegativitású atomok között alakul ki, mint például a vízmolekulában (H₂O), ahol az oxigén jelentősen elektronegatívabb, mint a hidrogén. Ilyenkor a közös elektronpár elmozdul az elektronegatívabb atom felé, így részleges töltések alakulnak ki a molekulában.
Ez a polaritás nagyban befolyásolja a molekulák oldhatóságát, fizikai tulajdonságait és reakcióképességét. Az apoláris molekulák általában nem oldódnak vízben, míg a polárisak igen.
A kovalens kötés polaritása meghatározza a közlekedőáramokat a sejtekben, a víz oldatként való viselkedését, a fehérjék szerkezetét és sok más biológiai, technológiai folyamatot.
Kötéshossz és kötéserősség az egyes típusoknál
A kovalens kötések kötéshossza azt jelöli, hogy a két összekapcsolódó atommag közötti távolság mekkora egy adott kötés típusánál. Az egyszeres kötés a leghosszabb, a kettős rövidebb, a hármas pedig a legrövidebb.
A kötéserősség vagy kötési energia azt jelenti, hogy mennyi energia szükséges egy adott kötés felbontásához. Hasonlóan: az egyszeres kötés a leggyengébb, a kettős erősebb, a hármas a legerősebb.
Az alábbi jellemző értékek a szénatomok közötti kötésekre:
- C–C egyszeres kötés kötéshossza ≈ 154 pm, kötési energia ≈ 348 kJ/mol
- C=C kettős kötés kötéshossza ≈ 134 pm, kötési energia ≈ 614 kJ/mol
- C≡C hármas kötés kötéshossza ≈ 120 pm, kötési energia ≈ 839 kJ/mol
A kötéshossz és a kötéserősség is meghatározza a molekulák stabilitását, reakcióképességét, fizikai tulajdonságait (például olvadás- és forráspont).
Kovalens kötés típusok összehasonlítása táblázatban
| Kötéstípus | Kötő elektronpárok száma | Kötéshossz (pm) | Kötési energia (kJ/mol) | Rotáció lehetséges? | Példamolekula |
|---|---|---|---|---|---|
| Egyszeres | 1 | 154 | 348 | Igen | H–H, CH₄ |
| Kettős | 2 | 134 | 614 | Nem | O₂, C₂H₄ |
| Hármas | 3 | 120 | 839 | Nem | N₂, C₂H₂ |
Előnyök és hátrányok a kötéstípusok között
| Kötéstípus | Előnyök | Hátrányok |
|---|---|---|
| Egyszeres | Stabil, rugalmas szerkezet, könnyen kialakul | Kevésbé erős, némely esetben reaktív |
| Kettős | Erősebb, merevebb szerkezet, reakcióképesebb | Nem engedi a szabad rotációt, kevésbé stabil |
| Hármas | Legerősebb, legrövidebb kötés, nagy energia | Nehezen bontható, gyakran inert (tehetetlen) |
SI mértékegységek, átváltások és jelek
| Fizikai mennyiség | Jelölés | SI mértékegység | Átváltás, példa |
|---|---|---|---|
| Kötési energia | E | joule (J) | 1 kJ = 1000 J |
| Kötéshossz | d | méter (m) | 1 pm (pikometer) = 10⁻¹² m |
| Töltés | q | coulomb (C) | milli: mC = 10⁻³ C |
| Anyagmennyiség | n | mol | mikro: μmol = 10⁻⁶ mol |
Összegzés: a kovalens kötések szerepe a kémiában
A kovalens kötés típusainak – az egyszeres, kettős és hármas kötések – megértése alapvető fontosságú a kémia minden területén. Ezek a kötések határozzák meg nemcsak a molekulák szerkezetét, hanem azok tulajdonságait, reakcióképességét és szerepét az élő és élettelen természetben.
A kovalens kötések fajtái közötti különbségek a molekulák rugalmasságát, merevségét, energiaigényét és reakcióképességét is befolyásolják. Az egyszeres kötés stabilitást és rugalmasságot, a kettős kötés merevséget és nagyobb reaktivitást, a hármas pedig extrém stabilitást és energiatartalmat jelent.
A kovalens kötés típusainak ismerete nélkül elképzelhetetlen a modern kémia, a biológia, a gyógyszerészet vagy akár a mindennapi anyagok szerkezetének megértése. A gyakorlati életben és a tudományban is kulcsszerepük van, legyen szó egyszerű gázokról, vízről vagy bonyolult szerves molekulákról.
GYIK – Gyakran Ismételt Kérdések
-
Mi a kovalens kötés lényege?
- Két atom közös elektronpár(oka)t oszt meg egymással stabilabb elektronszerkezet kialakítására.
-
Miben különbözik az egyszeres, kettős és hármas kötés?
- Az elektronpárok számában: egyszeresnél egy, kettősnél kettő, hármasnál három közös elektronpár van.
-
Miért erősebb a hármas kötés, mint az egyszeres?
- Több közös elektronpár szorosabban tartja össze az atomokat, rövidebb a kötéshossz.
-
Milyen molekulákban található kettős kötés?
- Például oxigén (O₂), szén-dioxid (CO₂), etén (C₂H₄) molekulákban.
-
Lehet polaritása egy kovalens kötésnek?
- Igen, ha az atomok elektronegativitása eltér, poláris lesz a kötés.
-
Miért nem forog szabadon a kettős és hármas kötés mentén a molekula?
- A π-kötés(ek) jelenléte merev szerkezetet ad.
-
Mi az egyszeres kovalens kötés fő jellemzője?
- Egy elektronpár, stabil, rugalmas kötésszerkezet.
-
Hogyan jelöljük a kovalens kötések típusait szerkezeti képletekben?
- Egyszeres: egy vonal (–), kettős: két vonal (=), hármas: három vonal (≡).
-
Miért fontos a kovalens kötés a technológiában?
- Anyagok, műanyagok, gyógyszerek, üzemanyagok szerkezetét és tulajdonságait határozza meg.
-
Melyik kovalens kötés a leghosszabb és melyik a legrövidebb?
- Az egyszeres kötés a leghosszabb, a hármas a legrövidebb.