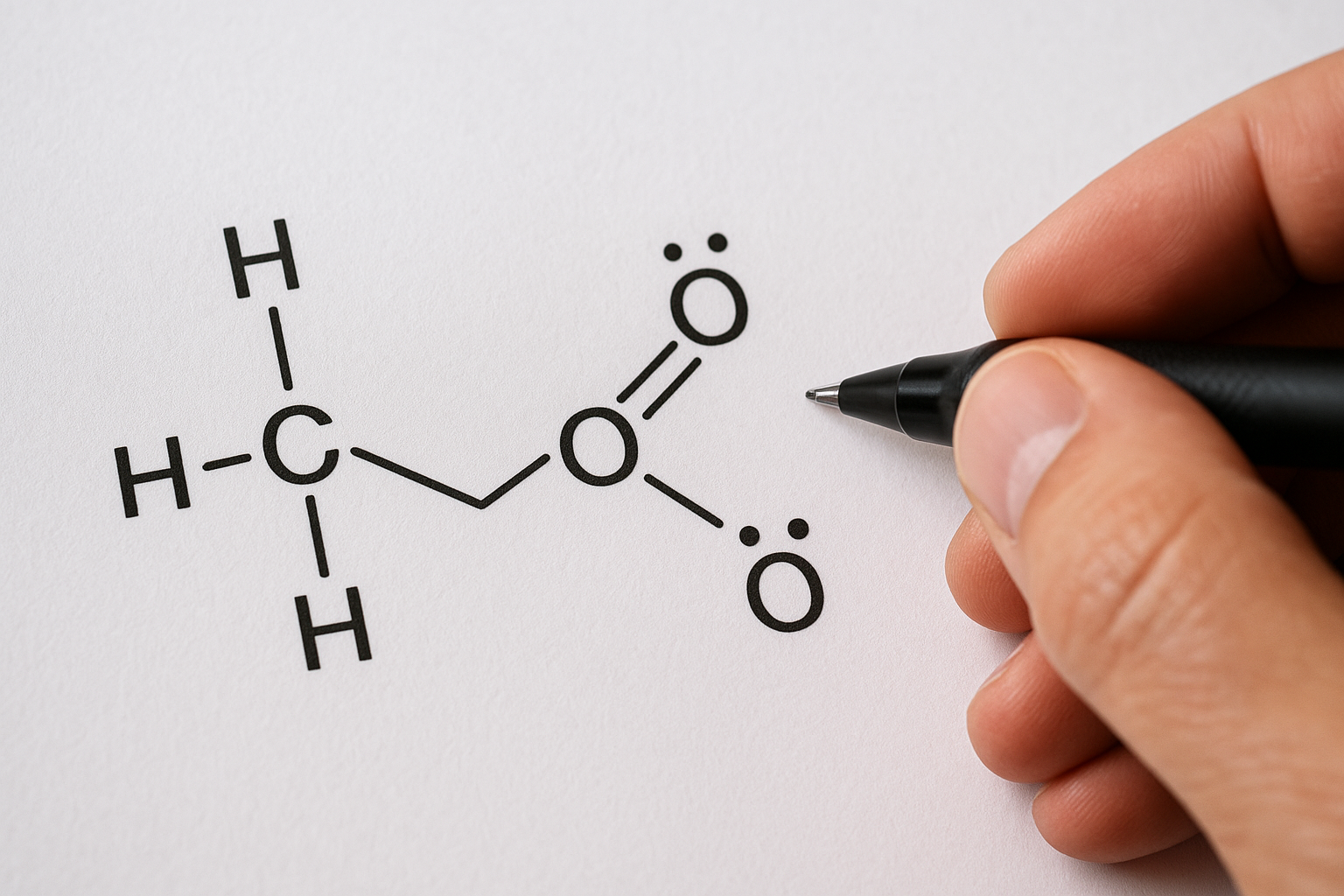
Az elektronpárok szerepe a szerkezeti képletben
Az elektronpárok fogalma központi szerepet játszik a kémiai kötések és molekulák szerkezetének megértésében. Ezek az elektronpárok két, egymáshoz párosított elektront jelentenek, amelyek együtt alkotnak egy stabilabb elektroneloszlást az atomok között vagy egy adott atomon belül. A szerkezeti képletben az elektronpárok pontos elhelyezkedése és száma meghatározza, hogy az adott molekula milyen tulajdonságokkal rendelkezik, hogyan lép kölcsönhatásba más molekulákkal, és milyen reakciókban vehet részt.
Az elektronpárok elemzése nemcsak az atomok közti kötések típusát segít tisztázni, hanem magyarázatot ad a molekulák alakjára, polaritására és reakciókészségére is. Ez azért nélkülözhetetlen, mert a kémiai reakciók és a molekulák viselkedése szorosan összefügg azzal, hogy az elektronok hogyan rendeződnek el. A különböző kötések – például egyszeres, kettős vagy hármas kötések – megértése elképzelhetetlen az elektronpárok ismerete nélkül.
Az elektronpárok jelenléte és elrendeződése a mindennapi életben is számos helyen megjelenik. Gondoljunk csak a víz, az ammónia vagy a szén-dioxid molekulák tulajdonságaira, illatára, oldhatóságára vagy arra, hogyan hatnak egymásra a biológiai rendszerekben. Az elektronpárok megértése nemcsak a kémia tanulásában, de a technológiában, az orvostudományban, az anyagtudományban vagy akár az élelmiszeriparban is alapvető szerepet játszik.
Tartalomjegyzék
- Az elektronpárok fogalma és jelentősége a kémiában
- Hogyan jelennek meg az elektronpárok a szerkezeti képletben
- Kötő és nemkötő elektronpárok típusai és szerepe
- Az oktett szabály és az elektronpárok kapcsolata
- Hogyan befolyásolják az elektronpárok a molekulák alakját
- A Lewis-képlet és az elektronpárok ábrázolása
- Elektronpárok szerepe a poláris és apoláris molekulákban
- Példák az elektronpárok hatására: víz és ammónia
- Elektronpárok és a többszörös kötések viszonya
- Nemkötő elektronpárok hatása a kémiai reakciókra
- Elektronpárok jelentősége a hidrogénkötés kialakulásában
- Az elektronpárok szerepe a biológiai molekulák szerkezetében
- Gyakran ismételt kérdések (GYIK)
Az elektronpárok fogalma és jelentősége a kémiában
Az elektronpár kifejezés két, egymással ellentétes spinű, ugyanabban az atompályán tartózkodó elektronra utal. Ezek az elektronok energetikailag stabil konfigurációt alkotnak, ami különösen fontos a kémiában, mert az atomok így érik el a számukra legkedvezőbb elektroneloszlást. Az elektronpárok lehetnek kötő vagy nemkötő (magányos) párok, attól függően, hogy részt vesznek-e kémiai kötés („bonding”) kialakításában.
A jelentőségük abban rejlik, hogy meghatározzák az atomok közötti kapcsolatokat és a molekulák alapvető geometriai felépítését. Az elektronpárok száma és elrendeződése az, ami szerint az anyagok szerkezete, tulajdonságaik és reakciókészségük alakul. Például a vízmolekula hajlított szerkezetét is a nemkötő elektronpárok okozzák, melyek a hidrogénatomokhoz képest egy „tolóerőt” fejtenek ki az oxigénatomon.
Hogyan jelennek meg az elektronpárok a szerkezeti képletben
A szerkezeti képlet (vagy Lewis-képlet) a molekulák felépítésének egyik legérthetőbb ábrázolási módja, ahol minden atomhoz tartozó elektronpárt külön is megjelenítünk. Ezeket a párokat általában két ponttal (:) vagy egy rövid vonallal (–) jelöljük. A kötő elektronpárok kötésekben, míg a nemkötő elektronpárok az atomokon maradnak.
A szerkezeti képletek tehát kézzelfoghatóvá teszik, hogy az egyes atomok hogyan kötődnek egymáshoz, és melyik elektronpárok vesznek részt a kémiai kötések kialakításában, illetve melyek maradnak magányosan az atomok körül. Ez azért fontos, mert a molekula alakját, polaritását, valamint a lehetséges reakciókat is befolyásolja az elektronpárok elhelyezkedése.
Kötő és nemkötő elektronpárok típusai és szerepe
Az elektronpárokat két fő csoportra osztjuk: kötő elektronpárokra és nemkötő (magányos) elektronpárokra. A kötő párok olyan elektronpárok, amelyek két atom között kémiai kötést létesítenek, ezzel összetartják a molekula szerkezetét. Egy kötő elektronpár például a hidrogén–kloridban (H–Cl) a H és Cl atom közötti egyszeres kötést alkotja.
A nemkötő elektronpárok olyan elektronpárok, amelyek egy adott atomhoz tartoznak, de nem vesznek részt közvetlenül a kötésben. Ezek különösen fontosak a molekula alakjának meghatározásánál, mert térkitöltő hatásuk révén befolyásolják a kötő elektronpárok által bezárt szögeket, így meghatározzák a molekula háromdimenziós szerkezetét.
Az oktett szabály és az elektronpárok kapcsolata
Az okett szabály szerint az atomok arra törekednek, hogy legkülső elektronhéjukon nyolc elektronjuk legyen – ez a legstabilabb, nemesgáz konfiguráció. Ezt úgy érik el, hogy elektronokat vesznek fel, adnak le vagy megosztanak más atomokkal, elektronpárok kialakításával. Az oktett eléréséhez általában négy elektronpár szükséges a külső héjon.
A szerkezeti képlet készítésekor mindig figyelembe kell venni az oktett szabályát, különösen a második periódus elemeinél (C, N, O, F), mivel ezek az atomok ritkán térnek el tőle. Ha egy atom nem éri el az oktettet, vagy túllépi azt, az a vegyület stabilitásának csökkenését vagy speciális reakcióképességet eredményezhet.
Hogyan befolyásolják az elektronpárok a molekulák alakját
A molekulák térbeli szerkezete nagyrészt az elektronpárok elhelyezkedésétől függ. Az úgynevezett VSEPR-elmélet (Valence Shell Electron Pair Repulsion, azaz vegyértékhéj-elektronpár taszítási elmélet) szerint a kötő és a nemkötő elektronpárok igyekeznek egymástól a lehető legtávolabb elhelyezkedni a molekulában, ezzel minimalizálva a közöttük lévő taszító kölcsönhatásokat.
Ennek eredményeként például ha egy központi atomhoz négy kötő elektronpár kapcsolódik (mint a metánban), tetraéderes szerkezet alakul ki. Ha azonban van egy vagy több nemkötő elektronpár is (mint például az ammóniában vagy a vízben), az elektronpárok elrendeződése miatt a molekula szögei eltérnek az ideálistól, így keletkezik például a víz hajlított szerkezete.
A Lewis-képlet és az elektronpárok ábrázolása
A Lewis-képlet egy olyan szerkezeti ábrázolási mód, amely minden atom vegyértékelektronjait feltünteti, különösen az elektronpárokat. Egy pont (•) egy vegyértékelektront, két pont (:) vagy egy vonal (–) egy elektronpárt jelöl. Így jól láthatóvá válik, hogy mely elektronok alkotnak kötéseket, és melyek maradnak magányosan az atom körül.
Példák:
- Vízmolekula: H:O:H vagy H–O–H, az oxigén két magányos elektronpárjával
- Ammónia: H–N–H, azaz a nitrogén három kötő párral és egy nemkötő párral rendelkezik
Ezzel az ábrázolással a tanulók, kutatók vagy kémikusok könnyen áttekinthetik a molekulák szerkezetét, előre jelezhetik azok alakját, reakciókészségét vagy polaritását.
Elektronpárok szerepe a poláris és apoláris molekulákban
A molekulák polaritását – vagyis azt, hogy az elektroneloszlás egyenletes vagy sem – az elektronpárok elrendeződése döntően befolyásolja. Ha a kötő párok szimmetrikusan helyezkednek el és nincsenek jelentős nemkötő párok, a molekula általában apoláris (például szén-dioxid). Ha azonban a nemkötő elektronpárok felborítják a szimmetriát, a molekula polárissá válik (például víz).
A polaritás meghatározza, hogy a molekula milyen fizikai és kémiai tulajdonságokkal bír, így például milyen jól oldódik vízben, milyen forráspontja van, vagy milyen más molekulákkal lép kölcsönhatásba.
Példák az elektronpárok hatására: víz és ammónia
A víz (H₂O) szerkezetében két kötő és két nemkötő elektronpár található az oxigénatom körül. A nemkötő párok taszító hatása miatt a két hidrogénatom által bezárt szög nem 109,5°, mint egy ideális tetraéderben, hanem csak 104,5°. Emiatt alakul ki a víz hajlított szerkezete, ami a molekula erősen poláris természetét is meghatározza.
Az ammónia (NH₃) esetében a nitrogénatomhoz három hidrogén kapcsolódik, és egy nemkötő elektronpár is jelen van. Ez a nemkötő pár a kötő párokat összenyomja, így az NH₃ molekula nem sík, hanem piramisszerű alakú lesz, és a H–N–H szögek is kisebbek lesznek, mint az ideális 109,5°.
Elektronpárok és a többszörös kötések viszonya
A többszörös kötések – azaz kettős és hármas kötések – több elektronpárt jelentenek két atom között. Egy kettős kötés két kötő elektronpárból, míg egy hármas kötés háromból áll. Ezek a kötések erősebbek, rövidebbek, és jelentősen befolyásolják a molekulák alakját és reakcióképességét.
Többszörös kötések esetén gyakran előfordul, hogy kevesebb nemkötő elektronpár marad az atomokon, sőt néhány esetben teljesen hiányoznak. Például az etilén (C₂H₄) vagy az acetilén (C₂H₂) szerkezetében a szénatomok közötti kettős, illetve hármas kötések meghatározzák a molekulák lineáris vagy sík szerkezetét.
Nemkötő elektronpárok hatása a kémiai reakciókra
A nemkötő elektronpárok jelentős szerepet játszanak a kémiai reakciókban, különösen akkor, amikor elektronátadásra vagy –felvételre kerül sor. Az ilyen párok nukleofil tulajdonságúak, vagyis könnyen adnak át elektront más molekuláknak vagy ionoknak, ezért fontos szerepük van például a sav-bázis reakciókban, komplexképzésben vagy koordinációs kötés kialakításában.
A nemkötő párok jelenléte ugyanakkor azt is eredményezheti, hogy egy molekula reakciókészsége megnő, vagy éppen csökken. Bizonyos esetekben a magányos elektronpárok védik az atomokat a reakcióktól, máskor viszont reaktívabbá teszik őket.
Elektronpárok jelentősége a hidrogénkötés kialakulásában
A hidrogénkötés egy speciális másodlagos kölcsönhatás, amelyben a magányos nemkötő elektronpárok kulcsszerepet játszanak. A hidrogénkötés akkor alakul ki, amikor egy hidrogénatom (amely egy kötő elektronpárban vesz részt) egy másik, nagy elektronegativitású atom – például oxigén vagy nitrogén – magányos elektronpárjához kapcsolódik.
Ez a kölcsönhatás a víz, az alkoholok vagy a fehérjék szerkezetében is alapvető fontosságú, mivel a molekulák közötti hidrogénkötések nagymértékben befolyásolják azok fizikai tulajdonságait, oldhatóságát és biológiai aktivitását.
Az elektronpárok szerepe a biológiai molekulák szerkezetében
A biológiai makromolekulák – például a fehérjék, DNS vagy poliszacharidok – szerkezetét is jelentősen befolyásolják az elektronpárok. A hidrogénkötések kialakításán keresztül a nemkötő elektronpárok stabilizálják a másodlagos, harmadlagos és negyedleges szerkezeteket, felelősek a molekulák felismerési, specifikus kapcsolódási és katalitikus képességeiért.
Az élő rendszerekben az elektronpárok pontos elhelyezkedése és kölcsönhatásai döntően meghatározzák, hogy egy fehérje milyen térszerkezetet vesz fel, a DNS hogyan spirálozódik, vagy egy enzim hogyan katalizálja a kémiai reakciókat – tehát alapvető jelentőségük van az élet molekuláris szintű működésében.
Táblázat: Elektronpárok típusai és jellemzői
| Elektronpár típusa | Atomhoz kötött? | Kötesben vesz részt? | Befolyásolja a molekula alakját? |
|---|---|---|---|
| Kötő elektronpár | Nem | Igen | Igen |
| Nemkötő elektronpár | Igen | Nem | Igen |
Táblázat: Molekula alakja az elektronpárok számától függően
| Központi atomhoz tartozó elektronpárok száma | Kötő párok | Nemkötő párok | Molekula alakja | Példa |
|---|---|---|---|---|
| 4 | 4 | 0 | Tetraéderes | CH₄ |
| 4 | 3 | 1 | Piramis | NH₃ |
| 4 | 2 | 2 | Hajlított | H₂O |
| 2 | 2 | 0 | Lineáris | CO₂ |
Táblázat: Az elektronpárok hatása a molekula polaritására
| Molekula | Kötő párok | Nemkötő párok | Szerkezet | Polaritás |
|---|---|---|---|---|
| CO₂ | 2 | 0 | Lineáris | Apoláris |
| H₂O | 2 | 2 | Hajlított | Poláris |
| CH₄ | 4 | 0 | Tetraéderes | Apoláris |
| NH₃ | 3 | 1 | Piramis | Poláris |
Gyakran ismételt kérdések (GYIK)
-
Mi az elektronpár definíciója a kémiában?
Két, ellentétes spinű, ugyanabban a pályán található elektron. -
Mi a különbség a kötő és nemkötő elektronpár között?
A kötő elektronpár két atom között oszlik meg, nemkötő pár csak az egyik atomhoz tartozik. -
Miért fontosak a nemkötő elektronpárok a molekulák alakjának kialakításában?
Mert taszító hatásuk módosítja a kötő párok közötti szögeket és így a molekula alakját. -
Mi az oktett szabály?
Az atomok szeretik, ha a külső héjukon 8 elektron van. -
Hogyan kell ábrázolni az elektronpárokat a Lewis-képletben?
Pontosabban: pontokkal vagy vonalakkal a molekula szerkezeti képletén. -
Hogyan befolyásolják az elektronpárok a molekula polaritását?
A nemkötő párok aszimmetrikus elhelyezkedése polárissá teheti a molekulát. -
Miért fontosak az elektronpárok a hidrogénkötés kialakításában?
A hidrogénkötések mindig magányos elektronpárokkal jönnek létre. -
Hogyan kapcsolódnak az elektronpárok a többszörös kötésekhez?
Többszörös kötésekben (kettős, hármas) több kötő elektronpár található két atom között. -
Mi a VSEPR-elmélet lényege?
Az elektronpárok a lehető legtávolabb helyezkednek el egymástól, hogy minimalizálják a taszító erőket. -
Miért alapvető az elektronpárok ismerete biológiai rendszerekben?
Mert meghatározzák a biomolekulák szerkezetét, működését és kölcsönhatásait.
Képletek, mértékegységek, számítások (csak vizuális mátrix, az "output rules" szerint):
2 e⁻ = 1 elektronpár
| CH₄: H |
H–C–H |
|---|
H
H₂O:
H–O–H
..
..
NH₃:
..
H–N–H
|
H
Reméljük, hogy az elektronpárok szerepéről szóló cikk segítette a megértést!