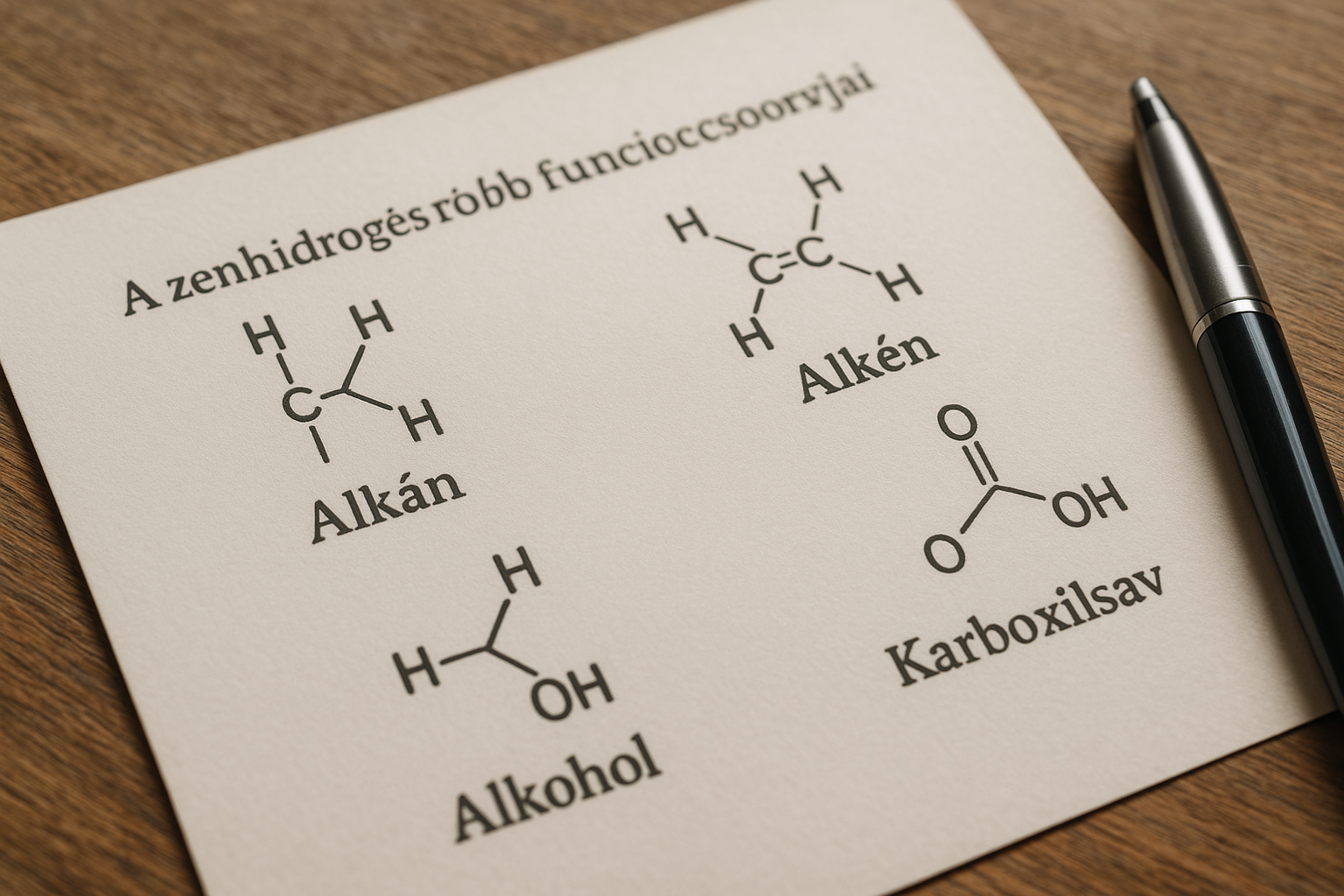
Bevezetés a szénhidrogének funkciós csoportjaiba
A szénhidrogének főbb funkciós csoportjai a szerves kémia alapvető építőkövei. Ezek a csoportok meghatározzák a molekulák kémiai tulajdonságait, reakciókészségét, és funkcionális lehetőségeit az élő szervezetekben, az iparban és a mindennapi életben. A funkciós csoportok felismerése, értelmezése és rendszerezése elengedhetetlen minden kémia szakos hallgató számára.
A téma fontossága abban rejlik, hogy minden szerves vegyület viselkedése a benne található funkciós csoportoktól függ. Ezek a csoportok határozzák meg, hogy egy adott molekula hogyan reagál más anyagokkal, milyen kölcsönhatásokra képes, és milyen ipari vagy biológiai szerepe lehet. A különböző funkciós csoportok ismerete nélkül lehetetlen lenne a szerves reakciókat vagy akár a bonyolult gyógyszermolekulákat megérteni és tervezni.
A funkciós csoportok szerepe a mindennapi technológiában is kiemelkedő: gondoljunk csak az üzemanyagokra, gyógyszerekre, műanyagokra vagy akár az élelmiszeripari adalékanyagokra. Mindenhol jelen vannak, ahol szerves vegyületek előfordulnak, felhasználásuk pedig folyamatos innovációt eredményez a vegyiparban és a kutatásban.
Tartalomjegyzék
- A szénhidrogének alapvető szerkezeti típusai
- Telített és telítetlen szénhidrogének bemutatása
- Az alkánok jellemzői és tipikus reakciói
- Az alkének szerkezete és funkcionális jelentősége
- Az alkinek sajátosságai és alkalmazási területei
- Aromás szénhidrogének és alapvető tulajdonságaik
- Halogénezett származékok: funkciók és felhasználás
- Alkoholok mint fontos funkciós csoportok
- Aldehidek és ketonok szerepe a szerves kémiában
- Karbonsavak tulajdonságai és gyakorlati jelentőségük
- Funkciós csoportok összefoglalása és jelentőségük
A szénhidrogének alapvető szerkezeti típusai
A szénhidrogének olyan szerves vegyületek, amelyek kizárólag szénből és hidrogénből épülnek fel. Ezek a molekulák lehetnek nyílt láncúak vagy gyűrűsek, attól függően, hogy a szénatomok milyen elrendezésben kapcsolódnak össze. A legegyszerűbb szénhidrogének az alkánok, amelyek csak egyszeres kötéseket tartalmaznak, míg a fejlettebb típusok kettős, hármas kötéseket, vagy speciális aromás szerkezeteket is mutathatnak.
A szénhidrogének csoportosítása az alábbiak szerint történik:
- Alkánok: csak egyszeres kötéseket tartalmaznak (például: metán, etán).
- Alkének: tartalmaznak legalább egy kettős kötést (például: etilén).
- Alkinek: tartalmaznak legalább egy hármas kötést (például: acetilén).
- Aromás szénhidrogének: speciális, gyűrűs szerkezetű vegyületek, mint a benzol.
Az alapszerkezet meghatározása elengedhetetlen, hiszen ez adja meg a kiindulópontot a különböző funkciós csoportok besorolásához és a további kémiai módosításokhoz.
Telített és telítetlen szénhidrogének bemutatása
A szénhidrogéneket telítettségük alapján két nagy csoportra oszthatjuk: telített és telítetlen vegyületekre. A telített szénhidrogének csak egyszeres kötéseket tartalmaznak minden szénatom között, ezáltal szerkezetük stabilabb, kevésbé reakcióképesek. Az alkánok tipikus példái ennek a csoportnak.
Ezzel szemben a telítetlen szénhidrogének – vagyis az alkének és alkinek – kettős vagy hármas kötéseket tartalmaznak, amelyek növelik a molekula reakciókészségét. Ezek a kötéseik miatt különleges kémiai reakciókra képesek, például addíciós reakciókra, ahol új atomok vagy molekulák csatlakozhatnak hozzájuk.
A telítettség kérdése nem csupán elméleti oldalról fontos, hanem praktikus szempontból is: például az élelmiszeriparban a telített és telítetlen zsírsavak elkülönítése a táplálkozástudomány egyik alappillére.
Az alkánok jellemzői és tipikus reakciói
Alkánok (paraffinok) azok a szénhidrogének, amelyekben a szénatomok között kizárólag egyszeres kötések találhatók. Ezek a vegyületek stabilak, kevéssé reakcióképesek, főként égési és szubsztitúciós reakciókra hajlamosak. Az alkánok általános képlete: CₙH₂ₙ₊₂.
Jellemző reakcióik közé tartozik az egyszerű égés (oxidáció), mely során szén-dioxid és víz keletkezik, valamint a halogénezés, ahol a hidrogénatomokat halogénatomokra cserélhetjük. Példa: a metán klórozása során klór-metán és hidrogén-klorid keletkezik.
Az alkánok fontos szerepet töltenek be az energetikában (földgáz, benzin), de a műanyaggyártásban, oldószerek előállításában is kiemelt jelentőségűek. Stabilitásuk miatt jól alkalmazhatók közegként más reakciókban is.
Az alkének szerkezete és funkcionális jelentősége
Az alkéneket a szénláncban előforduló legalább egy kettős kötés jellemzi. Ezek a kettős kötések lehetővé teszik, hogy az alkének reakcióképesebbek legyenek, különösen addíciós reakciókban. Általános képletük: CₙH₂ₙ.
A kettős kötés helye meghatározza a molekula izomerjeit (például 1-butén és 2-butén), ami a kémiai tulajdonságok megértéséhez elengedhetetlen. Az alkének például polimerizációs reakcióban is részt vehetnek, így polietilén vagy polipropilén is előállítható belőlük.
Az alkének a petrolkémia kiinduló anyagai, műanyagok, adalékok, kenőanyagok előállításában kulcsfontosságúak. A természetben is megtalálhatók, például növényi hormonok vagy természetes színanyagok alapvázaiként.
Az alkinek sajátosságai és alkalmazási területei
Az alkinek olyan szénhidrogének, amelyek legalább egy hármas kötést tartalmaznak a szénláncban. Ez a hármas kötés még reakcióképesebbé teszi őket az alkénekhez képest is. Az alkinek általános képlete: CₙH₂ₙ₋₂. A legismertebb alkinek az acetilén, melyet hegesztőgázként is használnak.
A hármas kötés miatt az alkinek molekulái lineáris szerkezetűek, ami különleges fizikai és kémiai tulajdonságokat kölcsönöz nekik. Addíciós reakcióik során először kettős, majd egyszeres kötésre redukálhatók, így sokféle vegyület előállítására alkalmasak.
Az alkinek jelentős ipari szerepet töltenek be: fontosak hegesztési technológiákban (oxiacetilén láng), műanyagiparban, és szintetikus gyógyszerek kiinduló anyagaiként is alkalmazzák őket.
Aromás szénhidrogének és alapvető tulajdonságaik
Az aromás szénhidrogének, főként a benzol és származékai, különleges stabilitású gyűrűs vegyületek, melyek delokalizált elektronrendszerrel rendelkeznek. Ez a delokalizáció a gyűrűs szerkezetben stabilitást biztosít, ugyanakkor speciális reakciókra is hajlamossá teszi ezeket a molekulákat.
Az aromás vegyületek főbb reakciója a szubsztitúció, például halogénezés vagy nitrálás. A benzol és származékai oldószerként, festékanyagok előállításánál, és sok gyógyszer alapvegyületeként is ismertté váltak. Az aromás vegyületek szerkezete, tulajdonságai és reakciómechanizmusai a szerves kémia külön fejezetét képezik.
Halogénezett származékok: funkciók és felhasználás
A halogénezett szénhidrogének olyan vegyületek, amelyekben a szénhidrogén-váz egyik vagy több hidrogénatomját halogénatomok (fluor, klór, bróm, jód) helyettesítik. Ezek a vegyületek nagyon változatos tulajdonságokkal rendelkeznek, attól függően, hogy melyik halogén található meg bennük.
Iparilag jelentős példák a klórozott vagy fluortartalmú szénhidrogének, amelyeket hűtőközegek, oldószerek, tűzoltó anyagok és műanyagok előállítására használnak. Fontos azonban környezeti szempontból is odafigyelni rájuk, hiszen egyes halogénezett származékok rendkívül tartósak és szennyező hatásúak (például freonok, DDT).
Alkoholok mint fontos funkciós csoportok
Az alkoholok olyan szénhidrogén-származékok, melyekben egy vagy több hidroxil-csoport (–OH) kapcsolódik a szénlánchoz. A legegyszerűbb alkohol a metanol, míg a legismertebb példák közé tartozik az etanol vagy az izopropanol. Az alkoholok általános képlete: CₙH₂ₙ₊₁OH.
Az alkoholok vízoldékonysága, forráspontja és reakciókészsége a hidroxil-csoportnak köszönhetően egészen különleges. Reakcióik, például oxidáció, észterképződés vagy dehidratálás, a mindennapi vegyiparban, élelmiszeriparban és gyógyszerészetben is kiemelt jelentőségűek. Emellett fontos oldószerek, fertőtlenítőszerek, tüzelőanyagok is.
Aldehidek és ketonok szerepe a szerves kémiában
Az aldehidek és ketonok szintén kulcsfontosságú funkciós csoportok. Ezekben a vegyületekben egy karbonil-csoport (C=O) található; különbség köztük, hogy az aldehidekben a karbonilcsoport láncvégi, míg a ketonokban láncközi helyzetű. Példák: formaldehid (aldehid) és acetón (keton).
Ezek a vegyületek jól definiált reakciókat mutatnak, például oxidációra, redukcióra, addícióra. Számos természetes vegyület és szintetikus anyag alapját képezik (pl. illatanyagok, gyógyszerek, oldószerek, polimerek).
Karbonsavak tulajdonságai és gyakorlati jelentőségük
A karbonsavak olyan szénhidrogén-származékok, amelyekben egy vagy több karboxil-csoport (–COOH) helyezkedik el. Ezek a legerősebb savak a szerves vegyületek között, és vízben jól oldódó, gyakran jellegzetes szagú anyagok. Például: ecetsav, citromsav.
A karbonsavak sói (karboxilátok) széles körben használatosak élelmiszeriparban, vegyiparban, gyógyszerészetben. A karbonsavak az élő szervezetek anyagcseréjében is kulcsszerepet játszanak (pl. zsírsavak, aminosavak).
Funkciós csoportok összefoglalása és jelentőségük
A szerves kémia világában a funkciós csoportok jelentik az egyediség forrását. Ezek a csoportok szabják meg, hogy egy adott molekula milyen tulajdonságokkal, reakciókészséggel és alkalmazási területtel rendelkezik. A főbb csoportok – alkánok, alkének, alkinek, aromás vegyületek, alkoholok, aldehidek, ketonok, karbonsavak, halogénezett származékok – mind más-más szerepet töltenek be az iparban, a környezetvédelemben, a biológiában és a mindennapi életben.
A funkciós csoportok ismerete minden kémikus számára alapvető fontosságú. Segítik az új vegyületek tervezését, reakciók levezetését és a környezetben előforduló folyamatok megértését. E tudás nélkül elképzelhetetlen lenne a modern vegyipar vagy akár az orvostudomány fejlődése.
Táblázatok
1. A főbb funkciós csoportok összehasonlítása
| Funkciós csoport | Jellemző csoport | Példa vegyület | Jellemző reakció | Felhasználás |
|---|---|---|---|---|
| Alkán | – | Metán | Égés, szubsztitúció | Üzemanyag, műanyag |
| Alkének | C=C | Etilén | Addíció, polimerizáció | Polietilén, adalék |
| Alkinek | C≡C | Acetilén | Addíció, égés | Hegesztőgáz, műanyag |
| Alkohol | –OH | Etanol | Oxidáció, észterképzés | Oldószer, fertőtlenítő |
| Aldehid | –CHO | Formaldehid | Oxidáció, addíció | Tartósítószer, műgyanta |
| Keton | –CO– | Acetón | Addíció, redukció | Oldószer, festék |
| Karbonsav | –COOH | Ecetsav | Sav-bázis, észterképzés | Konzerválás, élelmiszer |
| Halogénezett | –X (F, Cl, Br, I) | Klóretán | Szubsztitúció, elimináció | Hűtőközeg, oldószer |
| Aromás | Gyűrűs szerk. | Benzol | Szubsztitúció | Oldószer, festék |
2. Funkciós csoportok előnyei és hátrányai
| Funkciós csoport | Előnyök | Hátrányok |
|---|---|---|
| Alkánok | Stabilitás, jól égethető | Alacsony reakciókészség |
| Alkének | Reakcióképes, polimerizálható | Nehezebb tárolás, gyorsan polimerizálódik |
| Alkoholok | Oldékonyság, sokoldalú felhasználás | Égéshajlam, mérgező hatás (pl. metanol) |
| Ketonok | Jó oldószerek, stabilak | Gyúlékonyak, illékonyak |
| Halogénezett | Különleges tulajdonságok | Környezetszennyezők lehetnek |
3. Alkánok, alkének, alkinek főbb fizikai tulajdonságai
| Tulajdonság | Alkánok | Alkének | Alkinek |
|---|---|---|---|
| Olvadáspont | Alacsony | Alacsony | Alacsony |
| Forráspont | Növekszik a lánchosszal | Növekszik a lánchosszal | Növekszik a lánchosszal |
| Oldékonyság | Apoláris oldószerekben | Apoláris oldószerekben | Apoláris oldószerekben |
| Gyulladékonyság | Nagyon magas | Magas | Kiemelkedően magas |
| Reakciókészség | Kicsi | Közepes | Nagy |
GYIK – Gyakran ismételt kérdések
-
Mi a funkciós csoport jelentősége a szerves kémiában?
A funkciós csoport szabja meg a molekula kémiai tulajdonságait és reakciókészségét. -
Miben különbözik az alkán az alkéntől?
Az alkán csak egyszeres kötéseket tartalmaz, míg az alkén legalább egy kettős kötést. -
Milyen példát tudsz mondani aromás szénhidrogénre?
A benzol a legismertebb aromás szénhidrogén. -
Mire használják az alkoholokat?
Oldószerként, fertőtlenítőszerként és tüzelőanyagként is alkalmazzák őket. -
Mi a különbség az aldehid és a keton között?
Az aldehidben a karbonilcsoport láncvégi, a ketonban láncközi helyzetű. -
Milyen környezeti hatása lehet a halogénezett származékoknak?
Tartós szennyező anyagok lehetnek, például a freonok. -
Miért fontosak a karbonsavak a biológiában?
A zsírsavak és aminosavak szerkezeti alapjai. -
Mi a telítetlen szénhidrogén jelentősége?
Reakcióképesebbek, iparilag fontos kiinduló anyagok. -
Melyik a legreakcióképesebb szénhidrogén-típus?
Az alkinek, a hármas kötés miatt. -
Hogyan csoportosíthatók a szénhidrogének?
Telítettség, kötéstípus, szerkezeti forma és funkciós csoport alapján.