A konformáció fogalma: Mit jelent és miért fontos?
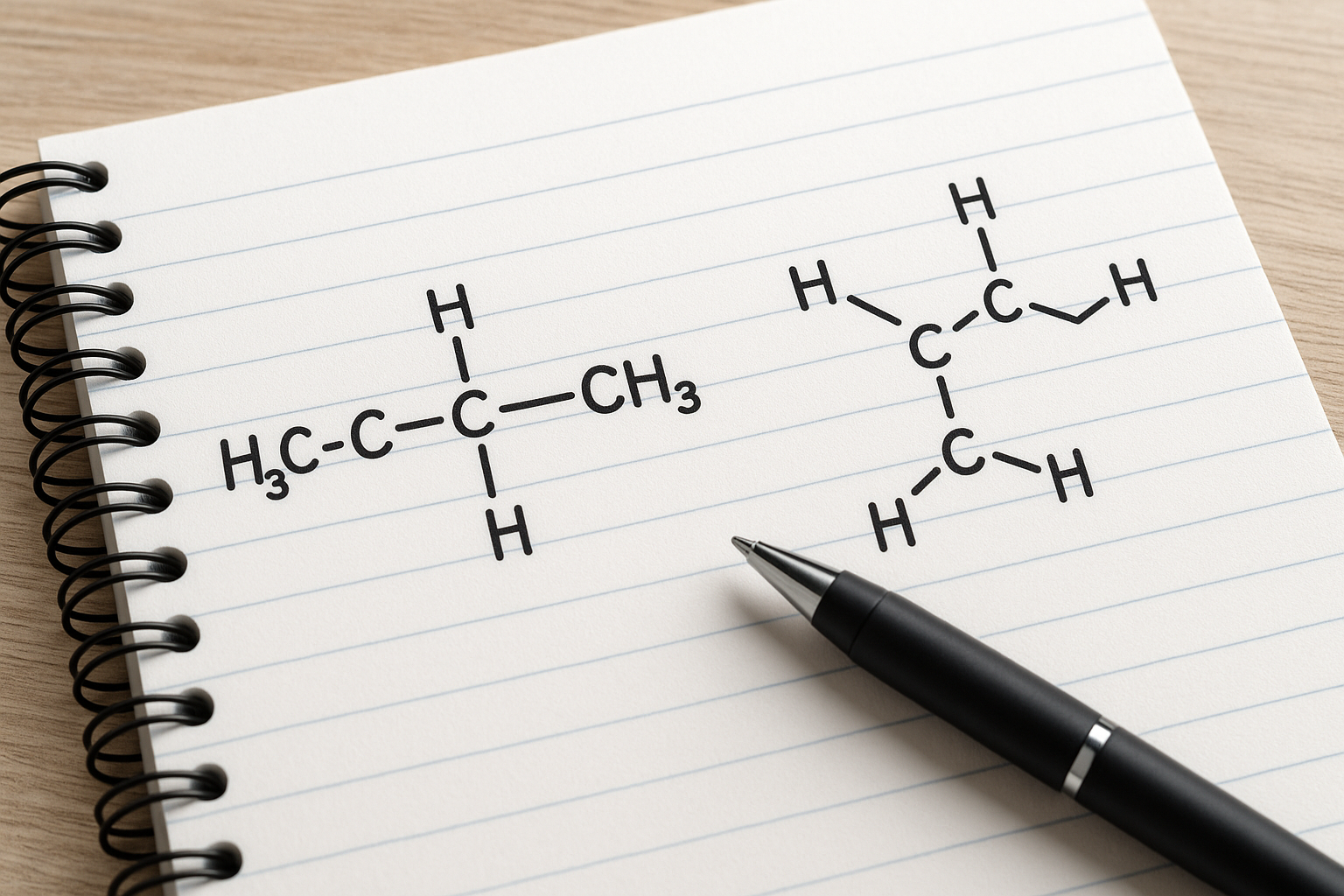
A konformáció a kémiai molekulák térbeli szerkezetének egy olyan változata, amely a kötések körüli elforgatás (rotáció) révén keletkezik, anélkül, hogy bármely kovalens kötés felbomlana. Ez azt jelenti, hogy egy adott molekula különböző „alakokat” vehet fel, miközben a szerkezeti képlete változatlan marad. A konformációs izoméria emiatt különösen fontos a szerves kémiában, mert a molekulák tulajdonságait és viselkedését alapvetően meghatározhatja.
A konformáció vizsgálata azért kiemelten jelentős a kémiában, mert a molekulák reakcióképessége, fizikai tulajdonságai (például olvadáspontja, oldhatósága), illetve biológiai aktivitása is szoros összefüggésben van azzal, hogy éppen milyen konformációt vesznek fel. Ezért a kémikusok számára elengedhetetlen, hogy megértsék, milyen tényezők befolyásolják a molekulák lehetséges konformációit, és miként lehet azokat vizsgálni.
A konformációs kérdések nem csak a laboratóriumban fontosak: mindennapi életünkben is számos helyen megjelennek. Gondoljunk például a fehérjék térbeli szerkezetére, a gyógyszerek hatásmechanizmusára, vagy akár az illatanyagok működésére. A modern gyógyszerek tervezése elképzelhetetlen lenne a konformációs analízis nélkül, hiszen a biológiai hatás gyakran egy-egy speciális molekula-alakhoz kötött.
Tartalomjegyzék
- A molekulák szerkezeti változékonysága
- A konformációs izoméria alapjai és típusai
- Energiagépek: Hogyan alakul ki a konformáció?
- Rotációs akadályok és azok jelentősége
- Leggyakoribb konformációk szerves vegyületekben
- A ciklohexán szék- és kád-konformációja
- Konformációk vizsgálata spektroszkópiával
- Hogyan befolyásolja a konformáció a reakciókat?
- Gyógyszerkutatás és konformációs analízis
- A konformáció szerepe a biológiai rendszerekben
- Összefoglalás: A konformáció jövőbeli kutatásai
A molekulák szerkezeti változékonysága
A kémiai molekulák nem merev, statikus objektumok, hanem állandó mozgásban lévő részecskék. Ez a mozgás nem csupán a helyváltoztatásra és a rezgésre, hanem a kötések menti rotációra is kiterjed. Ez utóbbi lehetőséget teremt arra, hogy a molekula különféle „alakokat”, vagyis konformációkat vegyen fel. Ez a változékonyság óriási jelentőségű, hiszen befolyásolja, hogy a molekula hogyan lép kölcsönhatásba más részecskékkel.
A konformációs flexibilitás legismertebb példái az egyszerű szénhidrogének, például az etán vagy a bután molekulái. Ezekben a szén-szén egyszeres kötések menti rotáció rendkívül könnyen megvalósul, így a molekula akár több milliárd konformációt is felvehet másodpercenként. Ezt a jelenséget mind a fizikai-kémiai reakciók, mind a biológiai folyamatok esetében figyelembe kell venni.
A konformációs izoméria alapjai és típusai
A konformációs izoméria, vagy konformerek jelenléte azt jelenti, hogy ugyanaz a molekula többféle térbeli elrendezést vehet fel a kötések mentén való elfordulás révén. Ezek az izoformák nem bonthatók meg normál hőmérsékleten kémiai kötés megszakítás nélkül, hanem egymásba alakulnak át a rotáció révén. A legismertebb példák között találjuk az etán „fedő” és „nyitott” konformációit.
A konformációs izoméria típusai közül a leggyakoribbak:
- Fedő (szinperiplánáris) konformáció: ahol a legnagyobb atomcsoportok fedik egymást.
- Átlapolt (antiklinális) konformáció: ahol a nagy atomcsoportok a lehető legmesszebb helyezkednek el egymástól.
- Göcsörtös (gauche) konformáció: amikor a csoportok térben egymáshoz közelebb kerülnek, de nem fedik egymást.
Mindegyik típus energetikailag eltérő stabilitású, ezért a molekulák jellemzően a legkedvezőbb, legalacsonyabb energiájú konformációt részesítik előnyben.
Energiagépek: Hogyan alakul ki a konformáció?
A konformációs változások hátterében az energia összetevőinek finom egyensúlya áll. A szén-szén egyszeres kötés körüli rotáció során a molekula potenciális energiája folyamatosan változik. Ez azt jelenti, hogy bizonyos konformációk stabilabbak, míg mások energetikailag kevésbé kedvezők.
Az etán molekulában például a fedő konformáció energiája magasabb, mert a hidrogének elektronfelhői között taszítás lép fel. A nyitott, vagyis átlapolt konformációban viszont ezek a taszító hatások minimálisak, ezért ez a szerkezet stabilabb. A konformációs energia-diagram ezt a változást szépen szemlélteti: a különböző konformerekhez eltérő energiaérték tartozik, és a molekula mindig a legalacsonyabb energiájú állapot felé törekszik.
Rotációs akadályok és azok jelentősége
A rotációs akadály egy adott kötés körül azt fejezi ki, hogy mekkora energia szükséges ahhoz, hogy egyik konformációból a másikba jussunk. Ez az energia elsősorban a kötések menti elektronfelhők átfedése miatt alakul ki. Minél nagyobb az akadály, annál lassabb a konformációs átalakulás.
A rotációs akadály jelentősége abban áll, hogy ha nagyon magas, akkor bizonyos konformációk „rögzülhetnek”, és így a molekula viselkedése gyökeresen eltérhet a szabadon forgó társaitól. Ez különösen fontos például a fehérjék másodlagos szerkezetének kialakulásánál, vagy akár az optikai izoméria megléténél. Egyes esetekben a rotációs akadály teszi lehetővé a molekulák „emlékezetét” is.
Leggyakoribb konformációk szerves vegyületekben
A szerves kémiában a legegyszerűbb példát az etán molekula nyújtja:
- Fedő konformáció: a két szénatomhoz kapcsolódó hidrogének egymás mögött vannak, nagy az elektronfelhő-átfedés.
- Átlapolt konformáció: a hidrogének egymástól a lehető legtávolabb helyezkednek el.
A bután esetében már három jelentős konformáció is elkülöníthető: az anti, a gauche és a szinperiplánáris. Ezek eltérő sajátságokkal rendelkeznek, például más-más a köztük levő energiakülönbség, illetve a reakcióképességük is változik.
A következő táblázat áttekintést ad a leggyakoribb konformációk előnyeiről és hátrányairól:
| Konformáció | Előnyök | Hátrányok |
|---|---|---|
| Átlapolt | Legstabilabb, alacsony energia | Nincs jelentős hátránya |
| Fedő | Könnyen kialakul | Magas energia, taszítás |
| Gauche | Egyes reakciókban előnyös | Köztes energia, sterikus akadály |
A ciklohexán szék- és kád-konformációja
A ciklohexán egy hat szénatomos, gyűrűs szénhidrogén, melynek konformációs viselkedése kiemelkedő jelentőségű a szerves kémiában. Ha síkban ábrázolnánk a ciklohexánt, torzulás jönne létre, és a kötésszögek eltérnének az ideálistól. Ezért inkább térben torzult szerkezeteket vesz fel – ezek a kád és a szék konformációk.
A szék-konformáció energetikailag sokkal kedvezőbb, mert minden szénatom tetraéderes geometriát vesz fel, és a hidrogénatomok között minimális a taszítás. A kád-konformáció ennél magasabb energiájú, kevésbé stabil. Az alábbi táblázat összefoglalja a két fő ciklohexán-konformáció fő különbségeit:
| Konformáció | Stabilitás | Energiatartalom | Előfordulás |
|---|---|---|---|
| Szék | Nagyon stabil | Alacsony | Domináns |
| Kád | Kevésbé stabil | Magas | Ritkább |
A ciklohexán konformációjának jelentősége abban is áll, hogy a szubstituált ciklohexánok esetében az oldalláncok helyzete (axiális vs. ekvatoriális) befolyásolja a molekula reaktivitását és fizikai tulajdonságait.
Konformációk vizsgálata spektroszkópiával
A modern kémia egyik legfontosabb eszköze a spektroszkópia, mely lehetővé teszi a molekulák térbeli szerkezetének, így a konformációjának a vizsgálatát. A leggyakrabban alkalmazott módszerek közé tartozik a magmágneses rezonancia (NMR) spektroszkópia és az infravörös (IR) spektroszkópia.
Az NMR segítségével például a hidrogénatomok közötti távolságokat, illetve a különböző konformációk arányát is meghatározhatjuk. Az IR-spektroszkópia érzékeny a molekula rezgési frekvenciáira, amelyek a konformáció függvényében változnak. Ezek a módszerek kulcsfontosságúak a szerkezetkutatásban, hiszen segítenek megérteni, hogyan változik a molekula szerkezete különböző körülmények között.
Hogyan befolyásolja a konformáció a reakciókat?
A kémiai reakciók menete nagyon gyakran függ attól, hogy a reagáló molekulák milyen konformációban találkoznak egymással. Az aktív konformációk azok, amelyek lehetővé teszik a leghatékonyabb kölcsönhatást, például a nukleofil támadást vagy az enzim-szubsztrát kapcsolódást.
Egy konkrét példa: a szubsztitúciós reakciókban a ciklohexán gyűrűn történő reakciók preferáltan az ekvatoriális pozícióban mennek végbe, mivel itt kisebb a sterikus akadály. Ezért a konformációs analízis elengedhetetlen a reakciómechanizmusok megértése szempontjából.
Gyógyszerkutatás és konformációs analízis
A gyógyszerkutatásban a konformációs analízis kritikus eszköz. Egy adott hatóanyag akkor fejti ki a kívánt biológiai hatást, ha pontosan illeszkedik a célfehérje aktív helyéhez – ezt nevezzük lock and key (zár és kulcs) modellnek. A molekula megfelelő konformációja nélkül a kötődés gyenge, vagy egyáltalán nem jön létre.
A modern számítógépes modellezés lehetővé teszi a potenciális hatóanyagok konformációs térképének felállítását, így célzottan kereshetők a legalkalmasabb szerkezetek. Ez jelentősen gyorsítja és hatékonyabbá teszi a gyógyszerfejlesztést. A következő táblázat az előnyöket és kihívásokat foglalja össze:
| Előnyök | Kihívások |
|---|---|
| Jobb célzott hatóanyag-fejlesztés | Nagy számítási igény |
| Gyorsabb hatóanyag-szűrés | Komplex kémiai térkép |
| Kevesebb mellékhatás | Pontos szerkezetismeret szükséges |
A konformáció szerepe a biológiai rendszerekben
A biológiai makromolekulák, például a fehérjék és nukleinsavak (DNS, RNS) funkciója elválaszthatatlanul kapcsolódik a konformációhoz. A fehérjék aktív helye csak a megfelelő térbeli szerkezet (konformáció) kialakulása után lesz képes ellátni feladatát. A fehérjék hibás konformációja betegségekhez, például prionbetegségekhez vezethet.
Az élő rendszerek dinamikusak: a fehérjék folyamatosan „lélegeznek”, kisebb-nagyobb konformációs változásokon mennek keresztül. Ezek a mozgások teszik lehetővé a biokémiai folyamatok szabályozását, például az enzimek aktiválását vagy gátlását. A konformációs egyensúly fenntartása ezért alapvető a szervezet normális működése szempontjából.
Összefoglalás: A konformáció jövőbeli kutatásai
A konformációs kutatások napjainkban is élénkek. Egyre több részlet derül ki arról, hogy mely tényezők befolyásolják a különböző molekulák szerkezeti flexibilitását. Az új, nagy felbontású szerkezetmeghatározó technikák (pl. krio-elektronmikroszkópia) lehetővé teszik a konformációk pontos megfigyelését nagy, komplex rendszerekben is.
A jövő kihívásai közé tartozik a konformációval vezérelt precíziós gyógyszertervezés, a bonyolult reakciómechanizmusok modellezése, valamint az élő rendszerek konformációs hálózatainak feltérképezése. A konformáció megértése kulcsot ad számos tudományág fejlődéséhez, a kémiától a biológián át az orvostudományig.
Kémiaképletek és számítások
Kémiai definíció:
A konformációk közti energia különbséget így írjuk fel etán esetén:
Eₐₖₐdály = Efedő − Eátlapolt
Szimbólumok és mennyiségek:
- E: energia (J vagy kJ)
- θ: torziós szög (° vagy rad)
- ΔE: energia különbség
Konformációs energia diagram:
Az energia-periódus változása egy teljes rotáció során:
E(θ) = E₀ + ½ × V × (1 − cos 3θ)
Egyszerű számítás:
Ha V = 12 kJ/mol és θ = 60°, akkor:
cos 180° = −1
E(60°) = E₀ + ½ × 12 × (1 − (−1))
E(60°) = E₀ + ½ × 12 × 2
E(60°) = E₀ + 12
SI mértékegységek és átváltások:
| Mennyiség | SI egység | Átváltás | Prefixum-példák |
|---|---|---|---|
| Energia | joule (J) | 1 kJ = 1000 J | kJ, MJ |
| Szög | fok (°), radián (rad) | 1 rad ≈ 57,3° | mrad, μrad |
| Távolság | nm, Ångström (Å) | 1 nm = 10 Å | pm, nm, μm |
GYIK – Gyakran Ismételt Kérdések
- Mi az a konformáció kémiai értelemben?
A molekula kötések menti rotációval létrejött, nem kötéstörésen alapuló izomerje. - Miért fontos a konformáció a gyógyszerkutatásban?
A hatóanyagok biológiai aktivitása gyakran konformáció-függő. - Mit jelent a rotációs akadály?
Az az energiamennyiség, amely szükséges egy kötés körüli elforgatással új konformációhoz jutni. - Melyik a legstabilabb konformáció az etánnál?
Az átlapolt konformáció, mert itt a hidrogének a legtávolabb vannak egymástól. - Hogyan mutatható ki egy adott konformáció?
Spektroszkópiás módszerekkel, például NMR-rel vagy IR-rel. - Mi a különbség a szerkezeti és a konformációs izoméria között?
A szerkezeti izoméria kötéstöréssel járó különbség, a konformációs pedig kötések mentén elfordulással. - Melyik a ciklohexán leggyakoribb konformációja?
A szék-konformáció a legstabilabb, ezért ez fordul elő leggyakrabban. - Befolyásolhatja-e a konformáció a reakciókét?
Igen, egyes konformációk kedvezőbbek a reakciók szempontjából. - Miért fontos a konformáció a biológiában?
A fehérjék és enzimek működéséhez elengedhetetlen a megfelelő konformáció. - Hogyan segíthet a konformációs analízis a tudományban?
Új anyagok, gyógyszerek tervezése, biológiai mechanizmusok megértése révén.