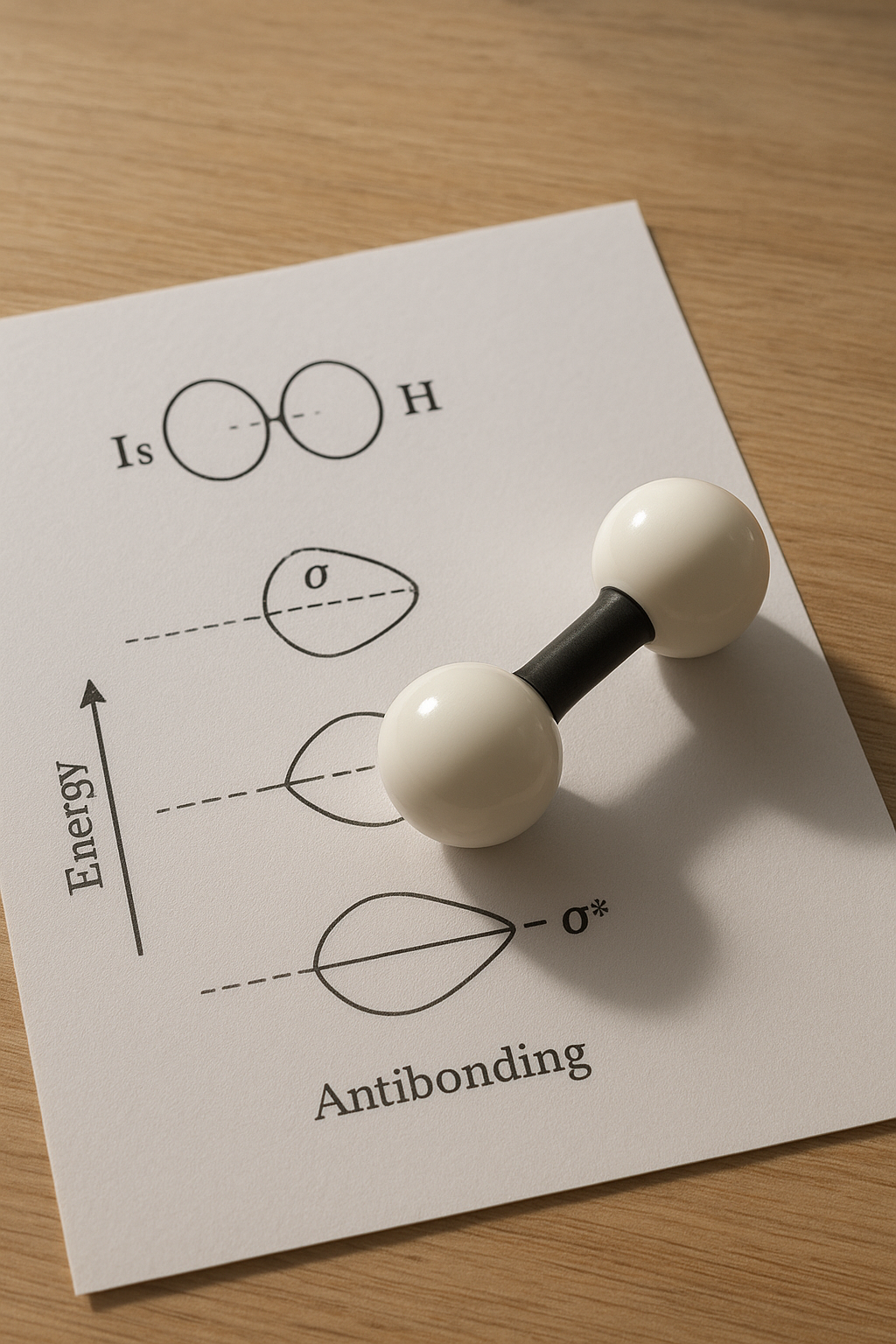
Molekulapálya-elmélet és a hidrogénmolekula
A molekulapálya-elmélet (MO-elmélet) a modern kémia egyik legfontosabb fogalma, amely azt írja le, hogyan helyezkednek el és mozognak az elektronok a molekulákban. Ezzel az elmélettel megérthetjük a kémiai kötések és a molekulák stabilitásának mélyebb okait – különösen a legegyszerűbb molekula, a hidrogénmolekula (H₂) esetében.
Az elmélet jelentősége abban rejlik, hogy képes magyarázatot adni olyan jelenségekre is, amelyeket a hagyományos szerkezeti képletek vagy a Lewis-féle képletrendszer nem tud. A molekulapálya-elmélet alkalmazása nélkül nem érthetnénk pontosan a kötések erősségét, a molekulák mágneses tulajdonságait vagy éppen az energetikai stabilitásukat.
Ez a tudás a hétköznapjainkban is jelen van: a hidrogénmolekula, mint a legkisebb és egyik leggyakoribb elem vegyülete, nélkülözhetetlen az üzemanyagcellák, a csillagok energiatermelése vagy a vegyipar folyamataiban. A molekulapálya-elmélet gyakorlati alkalmazásai nélkül ma nem létezne modern elektronikai vagy anyagtudományi ipar.
Tartalomjegyzék
- Mi az a molekulapálya-elmélet? Alapfogalmak bemutatása
- Az atomorbitálok és molekulapályák kapcsolata
- A hidrogénmolekula szerkezetének áttekintése
- Kötő és lazító molekulapályák jelentősége
- Elektronok elhelyezkedése a H₂ molekulában
- A molekulapálya-elmélet alkalmazása H₂-nél
- Energia és kötésrend fogalma a hidrogénmolekulában
- Kísérleti bizonyítékok a molekulapálya-elméletre
- A molekulapályák ábrázolása és vizualizációja
- A molekulapálya-elmélet korlátai és kritikái
- Összehasonlítás: Lewis-képlet és molekulapálya-elmélet
- A hidrogénmolekula jelentősége a kémiai kutatásban
Mi az a molekulapálya-elmélet? Alapfogalmak bemutatása
A molekulapálya-elmélet az elektronok viselkedését írja le molekulákban, azaz olyan rendszerekben, ahol több atom atommagja és elektronja találkozik. A lényeg, hogy a molekula egészéhez tartozó pályákat (molekulapályákat) vezet be, amelyek nem egyszerűen az atomok saját pályáinak összegei, hanem azok kombinációi. Ennek eredményeképpen új, delokalizált pályák jönnek létre, amelyek meghatározzák az elektronok eloszlását a molekulában.
Például a hidrogénmolekula (H₂) két hidrogénatomja egy-egy 1s pályával rendelkezik. Ezekből kétféle molekulapálya keletkezik: egy kötő és egy lazító, attól függően, hogy az atomorbitálok azonos vagy ellentétes fázisban szuperponálódnak. Ez a modern kémiai kötéselmélet egyik kulcseleme.
Az atomorbitálok és molekulapályák kapcsolata
Az atomorbitálok a mag körül kialakuló elektronfelhők, amelyekben nagy valószínűséggel tartózkodik az elektron. Ezek a pályák, például az s, p, d, f típusúak, egy atomon belül határozzák meg az elektron szerkezetét. Amikor két vagy több atom közel kerül egymáshoz, az orbitáljaik átfedhetnek, és új pályák – molekulapályák – jönnek létre.
A molekulapályák tehát olyan kvantummechanikai állapotok, amelyek a molekula egész atommag-rendszere körüli elektroneloszlást írják le. Ezek közül kiemelkedően fontosak a kötő (alacsonyabb energiájú) és a lazító (magasabb energiájú) pályák, amelyek meghatározzák, hogy a molekula stabil vagy instabil lesz-e.
A hidrogénmolekula szerkezetének áttekintése
A H₂ molekula a legegyszerűbb többatomos rendszer – két hidrogénatom kapcsolódik össze. Mindkét atom egy-egy elektront tartalmaz az 1s pályán. Amikor ezek az atomok közel kerülnek egymáshoz, a két 1s pálya lineárisan kombinálódik, így két új molekulapálya keletkezik: az egyik kötő, a másik lazító.
A kötő pálya (σ₁s) esetében az elektronok elektronfelhője két atommag között koncentrálódik, ezzel erősítve a kötést. A lazító pálya (σ*₁s) viszont a két mag közötti csomósíkkal rendelkezik, ahol az elektron sűrűsége minimális, vagyis a kötés gyengül.
Kötő és lazító molekulapályák jelentősége
A kötő molekulapályák olyan pályák, ahol az elektronok jelenléte erősíti a két atom közötti kötést: itt az elektron sűrűsége a két atommag között maximális. Ez stabilizálja a molekulát, mivel az elektronok a magok közé húzzák egymást, csökkentve a rendszer energiáját.
A lazító molekulapályák ennek éppen ellentétei: az ilyen pályákon elhelyezkedő elektronok gyengítik vagy akár meg is szüntethetik a kötést. Ezeken a pályákon a két atommag között csomósík található, ahol az elektron sűrűsége minimális. Az ilyen elektronok a magokat egymástól taszítják, növelve a rendszer energiáját.
Elektronok elhelyezkedése a H₂ molekulában
A hidrogénmolekula két elektronja a kötő (σ₁s) molekulapályán helyezkedik el, mivel ez az alacsonyabb energiájú pálya. Ez a konfiguráció a lehető legstabilabb, hiszen a két elektron közvetlenül a két mag között tartózkodik, maximalizálva a vonzó erőt a magok között.
A lazító pálya (σ*₁s) a következő elérhető energiaállapot, de normál állapotban ebbe nem kerül elektron a H₂ molekulában. Ha azonban energia (például fény) hatására a molekula gerjesztett állapotba kerül, előfordulhat, hogy az egyik elektron átugrik erre a pályára, ami a molekula szétbomlásához vezethet.
A molekulapálya-elmélet alkalmazása H₂-nél
A H₂ molekula az MO-elmélet egyik klasszikus példája. A két atom 1s pályájából a következő molekulapályák jönnek létre:
σ₁s
σ*₁s
A két elektron a σ₁s pályán helyezkedik el. Ez azt jelenti, hogy a kötésrend 1 (azaz egy szimpla kötés), és a molekula kötött állapotban van. Ezt az egyszerű modellt minden diák könnyen elképzelheti, és így a hidrogénmolekula stabilitása is világosan levezethető.
Az MO-elmélet lehetővé teszi annak megjóslását is, hogy mi történik, ha a molekulába más elektronok kerülnek, vagy ha a molekula gerjesztett állapotba jut. A H₂⁺ ion szerkezete például azért stabil, mert egy elektron még mindig a kötő pályán van, így létezhet a kationos forma is.
Energia és kötésrend fogalma a hidrogénmolekulában
A kötésrend megmutatja, milyen erős és hány elektronpár alkotja a kötést két atom között a molekulában. A kötésrend kiszámítható a molekulapályákon elhelyezkedő elektronok segítségével: a kötő pályán lévő elektronok számából kivonjuk a lazító pályán lévő elektronok számát, majd az eredményt elosztjuk kettővel.
Az energia szempontjából a kötő pálya alacsonyabb, a lazító pálya magasabb szintet képvisel. Ezért a két elektron a kötő pályán stabil állapotot biztosít, míg a lazító pálya betöltése a molekula bomlását okozhatja.
Kötésrend számítása:
(kötő elektronszám − lazító elektronszám) ÷ 2
H₂ molekulánál:
2 − 0 ÷ 2 = 1
Kísérleti bizonyítékok a molekulapálya-elméletre
A molekulapálya-elmélet helyességét kísérletek igazolják. Például az elektronspin-mérések vagy mágneses tulajdonságok vizsgálata azt mutatja, hogy a H₂ molekula diamágneses, ami azt jelzi, hogy minden elektron párosított, és a lazító pályák üresek – pontosan, ahogy az MO-elmélet jósolja.
Továbbá, spektroszkópiai mérések során a molekuláris energiaátmenetek is a várt módon jelennek meg: a gerjesztett állapotban az egyik elektron átkerül a σ*₁s pályára, ami megegyezik az elméleti várakozással. Az energia- és kötésrend-mérések szintén az MO-elméletet támasztják alá.
A molekulapályák ábrázolása és vizualizációja
A molekulapályák vizuális bemutatása segíti a tanulók és kutatók megértését. A kötő molekulapályát úgy ábrázoljuk, hogy az elektronfelhő egybefüggően öleli körül a két hidrogénmagot, sűrűsége a magok között a legnagyobb.
Ezzel szemben a lazító molekulapályán egy csomósík jelenik meg a két mag között, ahol az elektronfelhő megszakad, vagyis az elektron sűrűsége ott nulla. Az ilyen ábrázolások (például gömbhéj-modellek, elektroneloszlás-térképek, kontúrvonalas ábrák) minden tankönyvben vagy digitális kémiai modellező programban elérhetők.
A molekulapálya-elmélet korlátai és kritikái
Bár a molekulapálya-elmélet számos jelenséget sikeresen magyaráz, vannak esetek, amikor nem ad tökéletes választ. Különösen nagyobb molekulák vagy komplex rendszerek esetén az MO-elmélet számításai bonyolulttá válhatnak, és a valóságban tapasztalt kötésrend, mágnesesség vagy energia-értékek eltérhetnek az elméleti jóslatoktól.
További probléma, hogy a legegyszerűbb (lineáris kombinációs) MO-modellek nem tudják figyelembe venni az elektron-elektron taszítást, ami nagyobb molekuláknál jelentős lehet. Ezért a molekulapálya-elméletet gyakran kombinálják más kvantumkémiai módszerekkel, például a valenciakötés-elmélettel (VB-elmélet).
Összehasonlítás: Lewis-képlet és molekulapálya-elmélet
A Lewis-képlet egyszerű, jól áttekinthető módon ábrázolja a kovalens kötéseket: minden kötést egy vonal, minden nemkötő elektronpárt pedig pontok jelképeznek. Előnye, hogy gyorsan leolvasható a molekula szerkezete, de nem nyújt információt az elektronok pontos eloszlásáról vagy a kötés energetikai viszonyairól.
A molekulapálya-elmélet viszont mélyebb, kvantitatív képet ad a kötés természetéről, az elektronok energiaszintjeiről, pályáiról, és lehetővé teszi a kémiai és fizikai tulajdonságok pontosabb előrejelzését. Hátránya a bonyolultabb számítási igény és az absztraktabb szemlélet.
Összehasonlító táblázat: Lewis-képlet vs. molekulapálya-elmélet
| Szempont | Lewis-képlet | Molekulapálya-elmélet |
|---|---|---|
| Egyszerűség | Nagyon egyszerű | Komplex, matematikai |
| Elektron-eloszlás | Lokális (atomközi) | Delokalizált (molekula-szintű) |
| Kötésrend | Egyszerűen leolvasható | Számítható, pontosabb |
| Mágnesesség | Nem jósolható | Jósolható (párosítatlan elektronok) |
| Előrejelzések | Korlátozott | Nagy pontosságú |
A hidrogénmolekula jelentősége a kémiai kutatásban
A H₂ molekula alapvető szerepet tölt be a kémiai elméletek tesztelésében és fejlesztésében. Mivel a legegyszerűbb molekula, minden új kvantumkémiai modellt először ezen próbálnak ki a kutatók. Ezek az eredmények segítik a bonyolultabb molekulák leírását is.
Ezenkívül a hidrogénmolekula szerepe jelentős a modern technológiákban: üzemanyagcellák, csillagok energiatermelése, ipari hidrogén-előállítás – mind-mind ezen molekula kémiai és fizikai tulajdonságain alapulnak. A molekulapálya-elmélet adja ezekhez a folyamatokhoz a legpontosabb alapokat.
Táblázat: Molekulapálya-elmélet – Előnyök és hátrányok
| Előnyök | Hátrányok |
|---|---|
| Pontos elektronleírás | Komplex számítások |
| Előrejelzi a mágneses tulajdonságokat | Absztrakt szemlélet |
| Delokalizált pályák kezelése | Nagy molekuláknál nehézségek |
| Energetikai stabilitás magyarázata | Nem minden esetben pontos |
| Kísérleti eredményekkel egyezik | Egyszerűbb molekuláknál túlzott |
Táblázat: Molekulapályák főbb típusai
| Pálya típusa | Jelölés | Energia szint | Hatás a kötésre |
|---|---|---|---|
| Kötő | σ, π | Alacsony | Kötést erősít, stabilizál |
| Lazító | σ, π | Magas | Kötést gyengít, destabilizál |
| Nemkötő | n | Közepes | Semleges (nem változtat) |
Táblázat: SI-mértékegységek és előtagok a molekulapálya-elmélethez
| Mennyiség | Jelölés | SI-egység | Gyakori előtagok |
|---|---|---|---|
| Energia | E | joule (J) | kilo (kJ), milli (mJ), mikro (µJ) |
| Elektrontöltés | e⁻ | coulomb (C) | nano (nC), mikro (µC) |
| Kötésrend | — | dimenzió nélküli | — |
SI Egységek és átváltások
Az MO-elméletben az energia gyakori mértékegysége a joule (J), de a kémiai alkalmazásokban a kilojoule (kJ) és az elektronvolt (eV) is előfordul.
Átváltási példák:
1 kJ = 1000 J
1 eV ≈ 1,602 × 10⁻¹⁹ J
1 mJ = 0,001 J
1 µJ = 0,000001 J
A kötésrend azonban dimenzió nélküli mennyiség, csak a kötés erősségét mutatja.
Főbb képletek, szimbólumok, példák
Főbb szimbólumok:
- σ: szigma, vagyis tengelyszimmetrikus molekulapálya
- π: pí, vagyis oldalirányú átfedésű pálya
- **σ***: szigma-lazító pálya
- n: nemkötő pálya
- BR: kötésrend
- E: energia
Képletek:
Kötésrend:
(kötő elektronszám − lazító elektronszám) ÷ 2
Példa H₂ molekulánál:
2 − 0 ÷ 2 = 1
Gyakorlati számítási példa
Tegyük fel, hogy egy képzeletbeli H₂ molekulában négy elektron van:
Két a kötő, kettő a lazító pályán.
Kötésrend:
2 − 2 ÷ 2 = 0
Ez azt jelenti, hogy a molekula nem létezhet – valóban, a H₂²⁻ ion nem stabil.
GYIK – Gyakran Ismételt Kérdések
-
Mi a legfőbb különbség az atomorbitál és a molekulapálya között?
Az atomorbitál egy atom elektronfelhőjét, a molekulapálya viszont a teljes molekula elektroneloszlását írja le, több atom magjai körül. -
Miért fontos a kötő és lazító pályák fogalma?
Ezek szabják meg, hogy egy molekula stabil vagy instabil lesz, illetve, hogy milyen erős a kötés. -
Hogyan számoljuk ki a kötésrendet?
A kötő és lazító pályákon lévő elektronok számának különbségét kell elosztani kettővel. -
Mit jelent, ha a kötésrend nulla?
A molekula nem stabil, kötés nem alakul ki. -
Mikor jelenik meg lazító pályán elektron?
Gerjesztett állapotban vagy töltött ionok esetén, például H₂⁻. -
Mire jó a molekulapálya-elmélet a gyakorlatban?
Jósolja a molekula stabilitását, mágnesességét, energiaértékeit. -
Miért nem elég a Lewis-képlet?
Mert csak egyszerű, helyi kötéseket mutat, az energia- és mágnesességi viszonyokat nem. -
Milyen mértékegységeket használunk a molekulapálya-elméletben?
Joule, kilojoule, elektronvolt az energiára, de a kötésrendnek nincs egysége. -
Melyik molekula példája a legegyszerűbb az MO-elméletnek?
A hidrogénmolekula (H₂). -
Hol találkozhatunk a hidrogénmolekulával a technológiában?
Üzemanyagcellák, ipari vegyipar, csillagok energiatermelése.
Ez az összefoglaló segít az MO-elmélet alapjainak és a hidrogénmolekula szerkezetének megértésében, kezdőknek és haladóknak egyaránt!