A hidrogénmolekula kialakulásának alapjai
A hidrogénmolekula, kémiai jelöléssel H₂, a legegyszerűbb diatomos molekula, mely két hidrogénatomból épül fel. Ez a molekula alapvető szerepet tölt be a modern kémiában, az atomok közötti kovalens kötések tanulmányozásában és a kvantummechanikai modellek alkalmazásában. A hidrogénmolekula szerkezetének és kialakulásának megértése nélkülözhetetlen minden kémia szakos hallgató számára, hiszen számos további kémiai folyamat alapját képezi.
A hidrogénmolekula fontossága túlmutat a puszta kémiai elméleten: az univerzum legelterjedtebb molekulája, mely nemcsak a csillagközi térben fordul elő, hanem meghatározza a földi élet alapfolyamatait is. Energiatárolóként és üzemanyagként a technológiai ipar egyre fontosabb szereplőjévé válik, a fenntartható fejlődés egyik kulcsa lehet a jövőben.
A H₂ molekula kialakulásának részletes tanulmányozása lehetőséget teremt arra, hogy a diákok megértsék a kémiai kötés fogalmát, a molekulapályák viselkedését, valamint az energia- és stabilitásviszonyok jelentőségét. Az elméleti alapok mellett gyakorlati példák is segítik a tanultak elmélyítését, így a témakör nemcsak az alapok, hanem a haladó kémia szempontjából is elengedhetetlen.
Tartalomjegyzék
- A hidrogénmolekula szerepe a modern kémiában
- Az atomok szerkezetének rövid áttekintése
- Elektronpályák jelentősége a molekulákban
- A hidrogénatom elektronfelhőjének jellemzői
- Kovalens kötés: az alapfogalom bemutatása
- Hogyan jön létre a hidrogénmolekula?
- Az elektronpárok és a kötés kialakulása
- Energia- és stabilitásviszonyok a H₂ molekulában
- Molekulapálya-elmélet és a hidrogénmolekula
- A hidrogénmolekula kötési hosszának értelmezése
- A hidrogénmolekula keletkezésének energetikája
- A H₂ molekula jelentősége a tudományban és iparban
- Gyakran ismételt kérdések (GYIK)
A hidrogénmolekula szerepe a modern kémiában
A hidrogénmolekula (H₂) alapvető példája a kovalens kötésnek, amelyben két hidrogénatom oszt meg egy elektronpárt. Ez a legegyszerűbb molekula, mégis rendkívül fontos, mert minden további molekuláris kötések vizsgálatánál kiindulópontként szolgál. A hidrogénmolekula megértése segít a kémiai kötések, a molekuláris szerkezet, az energiaszintek és a kvantummechanikai leírások elsajátításában.
A modern kémiában a H₂ gyakorlati jelentőséggel is bír. A hidrogén, mint energiahordozó, fontos szerepet játszik az üzemanyagcellás technológiákban, a szerves szintézisekben, illetve a laboratóriumi kísérletekben. A hidrogénmolekula szerkezetének és reakcióképességének megértése tehát nemcsak elméleti, hanem gyakorlati szempontból is kulcsfontosságú.
Az atomok szerkezetének rövid áttekintése
Az atom szerkezete központi jelentőségű a kémia tanulásában. Egy atom magból és elektronfelhőből áll. A magban protonok és neutronok találhatók, míg az elektronok a mag körül, meghatározott pályákon (vagy energiaszinteken) helyezkednek el. A hidrogénatom a legegyszerűbb: egyetlen protont és egy elektront tartalmaz.
Az atomok viselkedését nagyban meghatározza az elektronhéjuk elrendeződése. Az elektronok vonzódnak a maghoz, de taszítják egymást. A stabil szerkezet eléréséhez az atomok hajlamosak elektronokat megosztani vagy átadni, amelyből különböző kémiai kötések (például kovalens, ionos) alakulnak ki. A hidrogénatom példája egyszerűsége miatt különösen jól használható a kötéselmélet magyarázatára.
Elektronpályák jelentősége a molekulákban
Az elektronpályák (orbitálok) fogalma nélkülözhetetlen a molekulák szerkezetének megértéséhez. Az elektronok nem egyszerűen körpályákon keringenek a mag körül, hanem valószínűségi eloszlású térrészekben (azaz pályákon) találhatók. Ezek az orbitálok határozzák meg, hogyan viselkednek az atomok egymás közelében.
Egy molekula úgy jön létre, hogy két vagy több atom elektronpályái átfednek, és közös elektronfelhőt hoznak létre. A hidrogénmolekula esetében két 1s elektronpálya (azaz két gömbszimmetrikus elektronpálya) egyesül, így stabilabb energiaállapot jön létre. Ez az egyszerű példa segít megérteni, hogyan alakulnak ki összetettebb molekulák is.
A hidrogénatom elektronfelhőjének jellemzői
A hidrogénatom egyetlen elektront tartalmaz, amely az 1s pályán helyezkedik el. Az 1s pálya gömbszimmetrikus, vagyis az elektron megtalálásának valószínűsége minden irányban azonos a mag körül. Az elektronfelhő nem pontos pályát jelent, hanem egy olyan térrészt, ahol az elektron előfordulásának esélye a legnagyobb.
Ez a felhőalapú felfogás magyarázza, miért képes két hidrogénatom közeledni egymáshoz és közös elektronpárt kialakítani. A hidrogénatom elektronfelhőjének egyszerűsége lehetővé teszi, hogy a kovalens kötés és a molekulapályák leírása könnyen érthető és jól szemléltethető legyen.
Kovalens kötés: az alapfogalom bemutatása
A kovalens kötés olyan kémiai kötés, amelyben két atom közös elektronpárt tart fenn. Ez akkor alakul ki, amikor egyik atom sem képes teljesen átadni vagy elvonni az elektront, de mindkettő stabilabbá válik, ha megosztják. A hidrogénmolekula a legegyszerűbb példa erre, mert mindkét hidrogénatom egy-egy elektronnal rendelkezik, és együtt egy elektronpárt alkotnak.
Az ilyen kötés kialakulása során az atomok elektronpályái átfedik egymást. Ennek eredményeként a kötésben részt vevő elektronok a két mag között helyezkednek el, így mindkét atom számára előnyös, stabilabb állapot jön létre. A kovalens kötés erőssége és típusa alapvetően meghatározza a molekula tulajdonságait.
Hogyan jön létre a hidrogénmolekula?
A hidrogénmolekula keletkezése egyszerű, de szemléletes példa a kovalens kötés kialakulására. Két H-atom közeledésekor elektronfelhőik átfednek, lehetővé téve, hogy az elektronpár mindkét atomhoz tartozzon. A két mag közötti elektronfelhő vonzást hoz létre, ez tartja össze a molekulát.
A folyamat során a két hidrogénatom közös elektronpárt alkot, így mindkettő számára kialakul az energetikailag kedvező hélium-szerű elektronszerkezet. Ez a kötött állapot energiafelszabadulással jár, ami azt jelenti, hogy a H₂ molekula alacsonyabb energiájú és stabilabb, mint a két különálló hidrogénatom.
Az elektronpárok és a kötés kialakulása
A kovalens kötés lényege az elektronpárok megosztása. Az elektronpár nem „tartozik” egyik atomhoz sem kizárólagosan, hanem a két mag között helyezkedik el. Ez az elrendezés biztosítja, hogy mindkét atom elérje a stabil, telített elektronhéjat (hidrogén esetén ez a hélium-állapot).
A hidrogénmolekula esetében az elektronpár közös pályán, a két atommag között található. Ez a kötési mód igen erős, mivel az elektronok vonzzák mindkét magot, összetartva az atomokat. Az elektronpárok elhelyezkedése meghatározza a molekula geometriáját és tulajdonságait.
Energia- és stabilitásviszonyok a H₂ molekulában
A hidrogénmolekula kötése során energia szabadul fel. Amikor két hidrogénatom közeledik, az elektronfelhők átfedése révén a rendszer energiája csökken. Ez azt eredményezi, hogy a kialakult molekula stabilabb, mint a két különálló atom. A kötési energia az a mennyiség, amelyet fel kell használni a molekula szétszakításához.
A H₂ molekula kötési energiája kb. 436 kJ/mol. Ez jelentős energia, amely megmagyarázza, miért stabil a hidrogénmolekula, és miért nehéz egyszerű körülmények között két hidrogénatomot szétválasztani. A vegyületek kémiai stabilitásának megértésében kulcsszerepet játszik ez a fogalom.
Molekulapálya-elmélet és a hidrogénmolekula
A molekulapálya-elmélet (MO-elmélet) a modern kémiában kulcsfontosságú a molekulák szerkezetének megértésében. Az elmélet szerint az atomi pályákból (orbitálokból) molekulapályák keletkeznek, amikor atomok közelítenek egymáshoz. Ezek a pályák lehetnek kötő vagy lazító karakterűek.
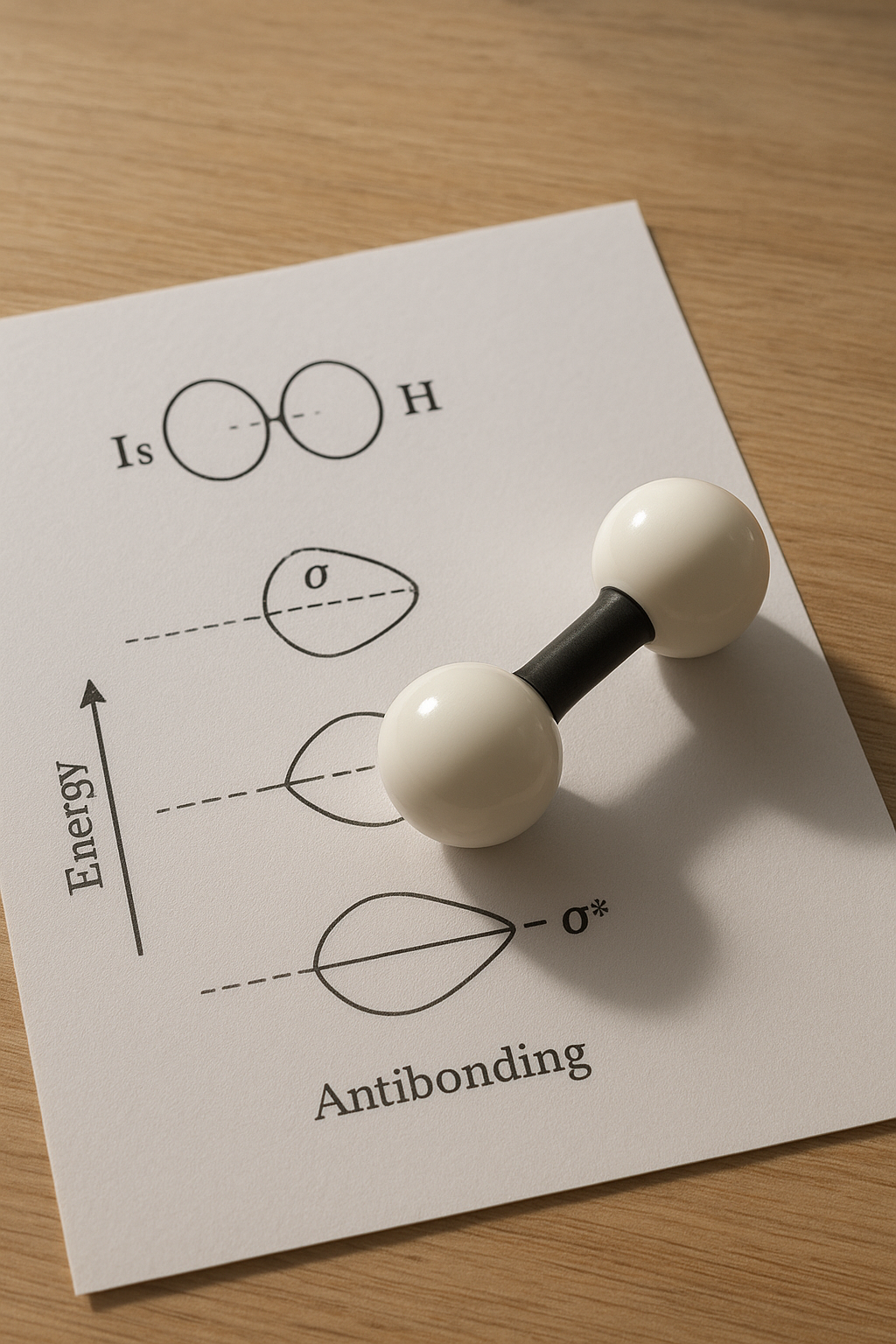
A H₂ esetében két 1s pálya egyesül, és két molekulapálya keletkezik: egy kötő (σ₁s) és egy lazító (σ*₁s) pálya. A két elektron a kötő pályán helyezkedik el, ami tovább stabilizálja a molekulát. Ha a lazító pályán is lenne elektron, a kötés gyengébb vagy nem létező lenne. Ez az elmélet világosan magyarázza, hogy miért stabil a H₂ molekula, és hogyan változna a szerkezet, ha több vagy kevesebb elektron lenne.
A hidrogénmolekula kötési hosszának értelmezése
A kötési hossz a két atommag közötti távolság egy molekulában. H₂ esetében ez az érték 74 pm (pikométer), amely a stabil energetikai állapotnak felel meg. Ez a távolság az, ahol a taszító és vonzó erők kiegyenlítik egymást, így a rendszer a legalacsonyabb energiájú konfigurációt veszi fel.
A kötési hossz azért fontos, mert meghatározza a molekula méretét és szerkezetét. Ha a magok közelebbi kerülnek, a taszító erők nőnek; ha távolabb, a vonzó erők gyengülnek, és a kötés megszűnik. A kötési hossz mérése és modellezése elengedhetetlen a molekulák tulajdonságainak kiszámításához.
A hidrogénmolekula keletkezésének energetikája
A hidrogénmolekula kialakulása során az energia változása kulcsfontosságú tényező. Amikor két hidrogénatom közelít egymáshoz, az elektronok és magok közötti kölcsönhatások elmozdítják a rendszer energiáját. A kötés kialakulásával az energia minimumhoz közelít, és energia szabadul fel.
A molekula kialakulásához szükséges energia (kötési energia) pontos mérése lehetővé teszi reakciók energetikájának előrejelzését, valamint a folyamatok hatékonyságának elemzését. Gyakran energetikai diagramokkal szemléltetjük, hogyan változik az energia a kötési hossz függvényében, bemutatva a stabil és instabil állapotokat is.
A H₂ molekula jelentősége a tudományban és iparban
A hidrogénmolekula tudományos jelentősége felmérhetetlen. Nemcsak a kémiai kötés fogalmának tanulmányozásához szolgál modellként, hanem alapvető szerepet játszik az asztrofizikában, a kvantummechanikai kutatásokban és a spektroszkópiában is. A H₂ szerkezetének kísérleti és elméleti vizsgálata a kémia és fizika határterületein is nélkülözhetetlen.
Az iparban a hidrogénmolekula kiemelt szerepet játszik. Az üzemanyagcellákban mint energiahordozó, a vegyiparban mint redukálószer, valamint az ammónia előállításában is alapvető fontosságú. Az új technológiák fejlődésével a hidrogénmolekula alkalmazási köre tovább bővül, kulcstényező lehet a fenntartható energiarendszerek kialakításában.
Táblázatok
1. A hidrogénmolekula előnyei és hátrányai
| Előnyök | Hátrányok |
|---|---|
| Egyszerű szerkezet | Nehezen tárolható |
| Könnyen modellezhető | Robbanásveszélyes |
| Alacsony tömeg | Korróziót okozhat |
| Nagy energia-tartalom | Speciális infrastruktúra kell |
| Gyors reakcióképesség | Drága előállítás |
2. A hidrogénmolekula fő jellemzői
| Jellemző | Érték |
|---|---|
| Képlet | H₂ |
| Kötési energia | 436 kJ/mol |
| Kötési hossz | 74 pm |
| Halmazállapot | Gáz |
| Molekulapályák | 1 σ₁s, 1 σ*₁s |
3. SI mértékegységek és prefixumok
| Mennyiség | SI egység | Prefixumok példák |
|---|---|---|
| Energiatartalom | J (joule) | kJ (kilojoule), MJ |
| Hosszúság | m (méter) | pm (pikométer), nm |
| Anyagmennyiség | mol | mmol (millimol) |
Képletek
2H + energia → H₂
Eₖₒₜ = 436 kJ/mol
dₖₒₜ = 74 pm
Gyakran ismételt kérdések (GYIK)
- Mi a hidrogénmolekula?
A hidrogénmolekula két hidrogénatomból álló, kovalens kötéssel összetartott diatomos molekula. - Miért fontos a hidrogénmolekula a kémiában?
Mert a legegyszerűbb és legjobban tanulmányozott példája a kovalens kötésnek. - Hogyan alakul ki a H₂ molekula?
Két hidrogénatom közeledik egymáshoz, közös elektronpárt hoznak létre, így kovalens kötés keletkezik. - Mi a hidrogénmolekula kötési hossza?
74 pikométer. - Mekkora a hidrogénmolekula kötési energiája?
436 kJ/mol. - Milyen szerepe van a H₂-nek az iparban?
Üzemanyagcellákban, ammónia előállításában és redukálószerként használják. - Mi a molekulapálya-elmélet jelentősége?
Leírja, hogyan oszlanak meg az elektronok a kötő és lazító pályákon, meghatározva a kötés erősségét és stabilitását. - Miért nehéz a hidrogéngáz tárolása?
Mert könnyen szökik, kis molekulatömegű, és robbanásveszélyes. - Hogyan lehet előállítani hidrogénmolekulát?
Leggyakrabban vízbontással (elektrolízissel) vagy földgázból, magas hőmérsékleten. - Miért tekintjük a H₂-t az univerzum legelterjedtebb molekulájának?
Mert a csillagközi térben és a csillagok belsejében is óriási mennyiségben található.