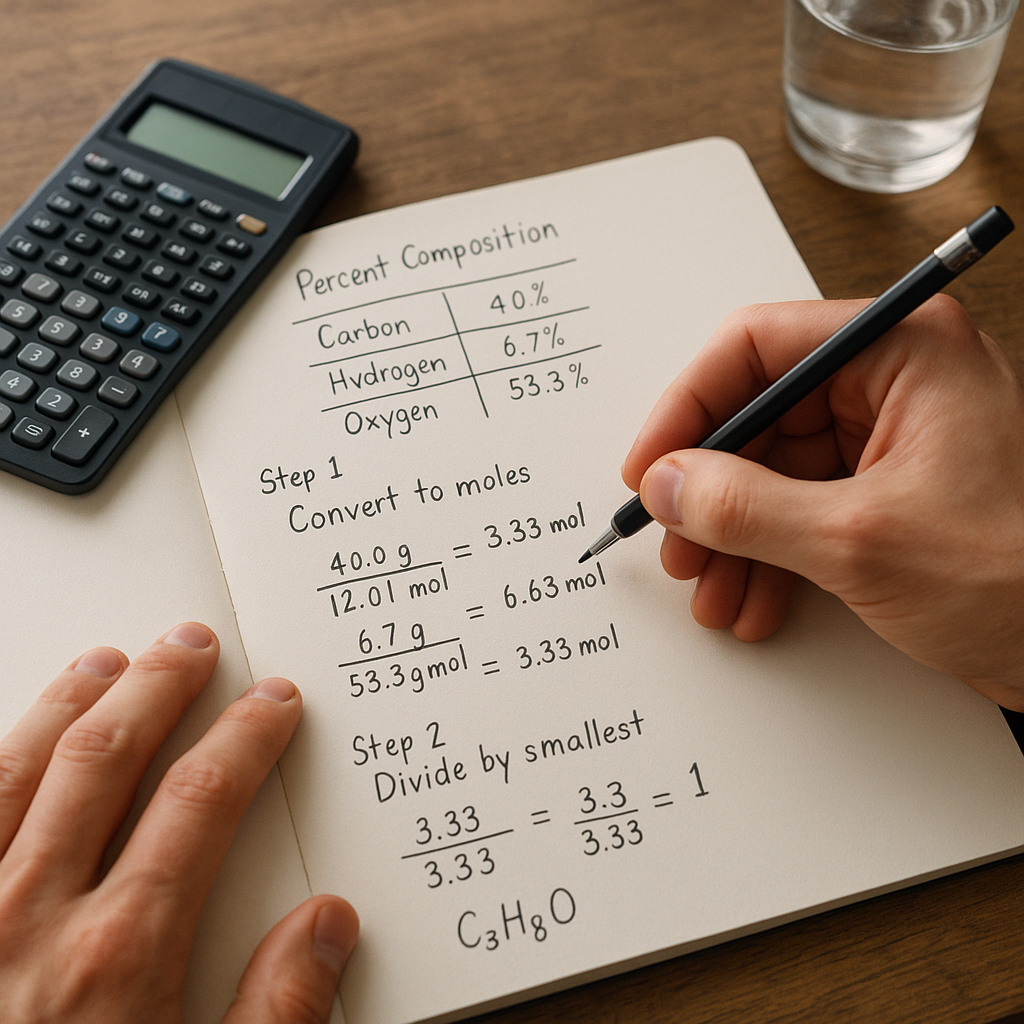Az empirikus képlet kiszámításának lépései
Az empirikus képlet a kémiában egy vegyület elemi összetételének legegyszerűbb, egész számú arányát adja meg. Lényegében megmutatja, hogy az adott vegyületben az egyes elemek atomjai milyen arányban találhatók meg egymáshoz képest. Az empirikus képlet meghatározása kulcsfontosságú lépés mind az analitikai, mind a szintetikus kémiában, hiszen ez az egyik leggyakrabban használt módszer ismeretlen vegyületek azonosítására.
Az empirikus képlet jelentősége abban rejlik, hogy segít felderíteni egy adott anyag összetételét, s ezzel hozzájárul a kémiai reakciók teljesebb megértéséhez és a vegyületek szerkezetének feltárásához. Ezen túlmenően, a képlet a molekulaképlet meghatározásának is kiindulópontja, különösen akkor, amikor csak korlátozott mennyiségű információ áll rendelkezésünkre egy anyag szerkezetéről.
A mindennapi életben az empirikus képlet kiszámítása elsősorban a gyógyszergyártás, az élelmiszeripar, az anyagvizsgálat és a környezetvédelem területén jelenik meg. Például, új gyógyszerhatóanyagok szerkezetvizsgálata, ismeretlen szerves vegyületek elemzése vagy akár egy szennyezőanyag azonosítása során elengedhetetlen módszer az empirikus képlet meghatározása.
Tartalomjegyzék
- Mi az empirikus képlet? Alapfogalmak áttekintése
- Az empirikus képlet jelentősége a kémiában
- Kiindulási adatok: tömeg vagy százalékarányok
- Az elemösszetétel tömegének meghatározása
- Az elemek mólszámának kiszámítása lépésről lépésre
- Mólszámok arányának egyszerűsítése
- Egyszerű egész számú arányok keresése
- Az empirikus képlet összeállítása az arányokból
- Ellenőrző számítás: helyesek az arányok?
- Különbség az empirikus és a molekulaképlet között
- Tipikus hibák és hogyan lehet elkerülni őket
- Az empirikus képlet kiszámításának gyakorlati példái
- GYIK (Gyakran ismételt kérdések)
Mi az empirikus képlet? Alapfogalmak áttekintése
Az empirikus képlet egy vegyületben jelen lévő elemek legkisebb egész számú arányát mutatja meg. Nem adja meg a tényleges atomok számát a molekulában (azt a molekulaképlet tartalmazza), hanem a legegyszerűbb arányt, amelyben az elemek jelen vannak. Például a hidrogén-peroxid empirikus képlete HO, míg a molekulaképlete H₂O₂.
A fogalom különösen fontos, mert gyakran először csak az elemek tömegaránya ismert egy ismeretlen anyagból. Az empirikus képlet kiszámítása ekkor az első lépés a vegyület pontos azonosítása felé. Ez az egyszerű képlet tömören összefoglalja a vegyület alapvető szerkezetét.
Az empirikus képlet jelentősége a kémiában
Az empirikus képlet meghatározása nélkülözhetetlen, amikor új vegyületeket vizsgálunk vagy ismeretlen anyagokat elemzünk. Gyakran ez az első lépés a szerkezetmeghatározás irányába, amely segít leszűkíteni a szóba jöhető vegyületek körét. A pontos empirikus képlet ismerete lehetővé teszi az analitikus kémikusok számára, hogy további szerkezeti vizsgálatokat végezzenek.
Számos területen, például a gyógyszerkutatásban, az élelmiszeranalitikában vagy a környezetvédelemben is kulcsszerepet játszik. Például, ha egy vízmintában felfedezett szennyező anyagról csupán az elemi összetétel ismert, az empirikus képlet adhat kiindulási pontot a további vizsgálatokhoz.
Kiindulási adatok: tömeg vagy százalékarányok
Az empirikus képlet kiszámításához kétféle kiindulási adat állhat rendelkezésre: az elemek tömege (grammban) vagy azok tömegszázalékos aránya. Ha a vegyület teljes tömege és az egyes elemek tömege ismert, ezekkel dolgozunk tovább. Amennyiben csak százalékos arányokat kapunk (például 40% szén, 6,7% hidrogén, 53,3% oxigén), először egy képzeletbeli 100 g-os mintát feltételezünk.
Ennek azért van jelentősége, mert a százalékaránnyal könnyen kiszámíthatjuk az egyes elemek tömegét egy 100 g-os minta esetén. Ez leegyszerűsíti a további lépéseket, hiszen 40% szén azt jelenti, hogy 100 gramm mintában 40 gramm szén van.
Az elemösszetétel tömegének meghatározása
Első lépésként meg kell határoznunk, hogy mennyi (gramm) található az adott elemből a megadott mintában. Ha százalékokat kaptunk, egyszerűen az adott százalékot vesszük egy képzeletbeli 100 grammos mintára. Ha például a vegyület 45% szén, 7,5% hidrogén és 47,5% oxigén, akkor ezek tömege: 45 g C, 7,5 g H, 47,5 g O.
Ha közvetlenül az elemek tömege áll rendelkezésre, azokat használjuk fel. Ezek az adatok lesznek az alapjai a következő lépéseknek, amikor a mólszámokat számítjuk ki.
Az elemek mólszámának kiszámítása lépésről lépésre
Most minden egyes elem tömegét elosztjuk az adott elem relatív atomtömegével (a periódusos rendszer alapján). Ennek eredményeként megkapjuk, hány mól atom van jelen az adott mennyiségből. Ez a lépés kulcsfontosságú, mert csak a mólszámok teszik lehetővé az arányok összehasonlítását.
Például, ha 40 g szén van a mintában, és a szén relatív atomtömege 12, akkor: 40 g ÷ 12 g/mol = 3,33 mol szén. Ezt minden elemre elvégezzük.
Mólszámok arányának egyszerűsítése
A kapott mólszámokat mindig a legkisebb mólszámhoz viszonyítjuk, azaz minden mólszámot elosztunk a legkisebb értékkel. Így megkapjuk, hogy az egyes elemek milyen arányban vannak jelen egymáshoz képest.
Ez a lépés azért fontos, mert az empirikus képlet egész számokból áll. Ha az arányok nem egész számok (például 1,5:1), akkor minden arányértéket megszorozunk a megfelelő számmal (ebben a példában 2-vel), hogy egész számokat kapjunk.
Egyszerű egész számú arányok keresése
Miután elvégeztük a mólszámok arányának egyszerűsítését, gyakran előfordul, hogy tört számokat kapunk (például 1,5 vagy 2,33). Ilyenkor minden arányértéket megszorozunk egy számmal, hogy egész számokat kapjunk. A 1,5:1 például 3:2 arány lesz, ha kettővel szorozzuk.
Fontos, hogy minden arányértéket ugyanazzal a számmal kell szorozni, különben a képlet arányai torzulnak. Ezzel a módszerrel biztosítjuk, hogy az empirikus képlet mindig egész számokat tartalmazzon.
Az empirikus képlet összeállítása az arányokból
Miután meghatároztuk az egész számú arányokat, ezek alapján írjuk fel az empirikus képletet. Az arányoknak megfelelően minden elem szimbóluma után odaírjuk az adott számot. Például, ha a végső arány C:2, H:6, O:1, akkor a képlet C₂H₆O lesz.
Fontos, hogy az egyes indexek (alsóindexek) sorrendje a megszokott sorrendet kövesse: szerves vegyületeknél például először a szén, aztán a hidrogén, majd oxigén, nitrogén, stb.
Ellenőrző számítás: helyesek az arányok?
Mindig érdemes visszaellenőrizni a számításainkat. Ezt úgy tehetjük meg, hogy az empirikus képlethez tartozó tömegarányokat újra kiszámoljuk, majd összevetjük a kiindulási adatokkal. Ha eltérés van, érdemes ellenőrizni a számítási lépéseket, mert lehet, hogy egy kerekítési vagy mólszám-elosztási hiba fordult elő.
Ez a lépés különösen fontos vizsgákon vagy laboratóriumi elemzések során, mert a pontatlanságok jelentős hatással lehetnek a további következtetésekre.
Különbség az empirikus és a molekulaképlet között
Az empirikus képlet csak az elemi arányokat mutatja meg, míg a molekulaképlet az egyes elemek tényleges atomjainak számát írja le a molekulában. Például a glükóz empirikus képlete CH₂O, de a molekulaképlete C₆H₁₂O₆.
A molekulaképlet mindig az empirikus képlet egész számú többszöröse, de tartalmazhat több információt a vegyület szerkezetéről. Az empirikus képlet tehát jó kiindulópont, de nem feltétlenül ad teljes képet a vegyület valódi összetételéről.
Tipikus hibák és hogyan lehet elkerülni őket
Az empirikus képlet kiszámításánál gyakori hiba, hogy a mólszámokat nem viszonyítják helyesen egymáshoz, vagy elfelejtik minden arányt ugyanazzal a számmal szorozni a tört értékeknél. Hibás lehet az is, ha rossz atomtömegekkel számolunk, vagy pontatlanul adjuk meg a kiindulási adatokat.
Ezeket a hibákat elkerülhetjük alapos ellenőrzéssel, pontos adatbevitellel, valamint a periódusos rendszer helyes használatával. Érdemes minden lépés után leellenőrizni a köztes eredményeket, hogy időben észrevegyük az esetleges eltéréseket.
Az empirikus képlet kiszámításának gyakorlati példái
Nézzünk két konkrét példát!
1. példa:
Egy vegyület tartalmaz 40,0% szén, 6,7% hidrogén és 53,3% oxigén elemeket.
-
Képzeletbeli 100 g-os mintát veszünk:
C: 40,0 g
H: 6,7 g
O: 53,3 g -
Mólszámok:
C: 40,0 ÷ 12,0 = 3,33
H: 6,7 ÷ 1,0 = 6,7
O: 53,3 ÷ 16,0 = 3,33 -
A legkisebb mólszám: 3,33
Arányok:
C: 3,33 ÷ 3,33 = 1
H: 6,7 ÷ 3,33 ≈ 2
O: 3,33 ÷ 3,33 = 1 -
Empirikus képlet: CH₂O
2. példa:
Egy vegyület 69,6% vasat és 30,4% oxigént tartalmaz.
-
100 g-os mintát feltételezve:
Fe: 69,6 g
O: 30,4 g -
Mólszámok:
Fe: 69,6 ÷ 56 = 1,243
O: 30,4 ÷ 16 = 1,9 -
Legkisebb mólszám: 1,243
Fe: 1,243 ÷ 1,243 = 1
O: 1,9 ÷ 1,243 ≈ 1,53 -
Mindkét értéket 2-vel szorozzuk:
Fe: 2 × 1 = 2
O: 2 × 1,53 ≈ 3 -
Empirikus képlet: Fe₂O₃
Táblázatok
1. Mólszámképzés áttekintése
| Elem | Tömeg (g) | Relatív atomtömeg | Mólszám |
|---|---|---|---|
| C | 40,0 | 12,0 | 3,33 |
| H | 6,7 | 1,0 | 6,7 |
| O | 53,3 | 16,0 | 3,33 |
2. Tipikus hibák és megelőzésük
| Hiba típusa | Következmény | Megoldás |
|---|---|---|
| Rossz atomtömeg használata | Hibás mólszám | Ellenőrzés a periódusos rendszerben |
| Nem megfelelő arányszámítás | Téves empirikus képlet | Mindig ossz a legkisebb mólszámmal |
| Egész számú arányok helytelen kiszámítása | Tört értékű indexek | Szorozz megfelelő számmal |
| Rossz kiindulási adatok (tömeg, %) | Teljesen hibás képlet | Pontos mérés, ellenőrzés |
3. SI mértékegységek és átváltási táblázat
| Menyiség | SI egység | Jele | Gyakori prefixek | Átváltás példa |
|---|---|---|---|---|
| Tömeg | gramm (g), kg | g, kg | milli (mg), mikro (μg) | 1 g = 1000 mg |
| Anyagmennyiség | mól | mol | milli (mmol), mikro (μmol) | 1 mol = 1000 mmol |
| Arány | — | — | — | — |
GYIK (Gyakran Ismételt Kérdések)
-
Mi az empirikus képlet és mire jó?
Az empirikus képlet egy vegyület elemi összetételének legegyszerűbb egész számú arányát mutatja meg. Segít a vegyület azonosításában és szerkezetének feltárásában. -
Mi a különbség az empirikus és a molekulaképlet között?
Az empirikus képlet az elemek legegyszerűbb arányát, a molekulaképlet pedig a tényleges atomok számát adja meg a molekulában. -
Mit tegyek, ha a mólszámok aránya nem egész szám?
Szorozd meg az összes arányértéket egy olyan számmal, hogy egész számokat kapj. -
Miért fontos a legkisebb mólszámhoz viszonyítani?
Így kapjuk meg az elemek legegyszerűbb arányát, amely szükséges az empirikus képlethez. -
Hogyan használjuk a periódusos rendszert a számításoknál?
Az elemek relatív atomtömegét a periódusos rendszerből olvassuk ki a mólszám számításához. -
Milyen egységekkel dolgozunk az empirikus képlet meghatározásánál?
Grammban mérjük a tömeget, mólt használunk az anyagmennyiséghez. -
Mi a teendő, ha pontatlan adatokat kapunk a kiindulásnál?
Ellenőrizzük a méréseket és a számításokat, szükség esetén ismételjük meg őket. -
Lehet-e két különböző vegyületnek ugyanaz az empirikus képlete?
Igen, például az etil-alkohol (C₂H₆O) és a dimetil-éter (C₂H₆O) különböző vegyületek, de empirikus képletük azonos. -
Melyik a leggyakoribb hiba az empirikus képlet számításánál?
A tört arányok helytelen kerekítése vagy elhagyása. -
Hol hasznos az empirikus képlet kiszámítása a gyakorlatban?
Vegyianyag-azonosítás, gyógyszerkutatás, környezetvédelem, élelmiszeranalitika területén egyaránt fontos.
Matematikai képletek (iskolai formában):
Tömegszázalék → Tömeg (100 g mintára):
mₑₗₑₘ = tömegszázalék × 100 g ÷ 100
Mólszám számítása:
n = m ÷ M
Mólszámok aránya (egyszerűsítve):
Arány = nₑₗₑₘ ÷ legkisebb n
Egész számú arány elérése (példánál):
1,5 : 1 = 3 : 2
Empirikus képlet példa:
C : H : O = 1 : 2 : 1 → CH₂O
Ezzel teljes és gyakorlati útmutatót kaptál az empirikus képlet kiszámításához, amely mind kezdők, mind haladók számára biztonsággal használható!