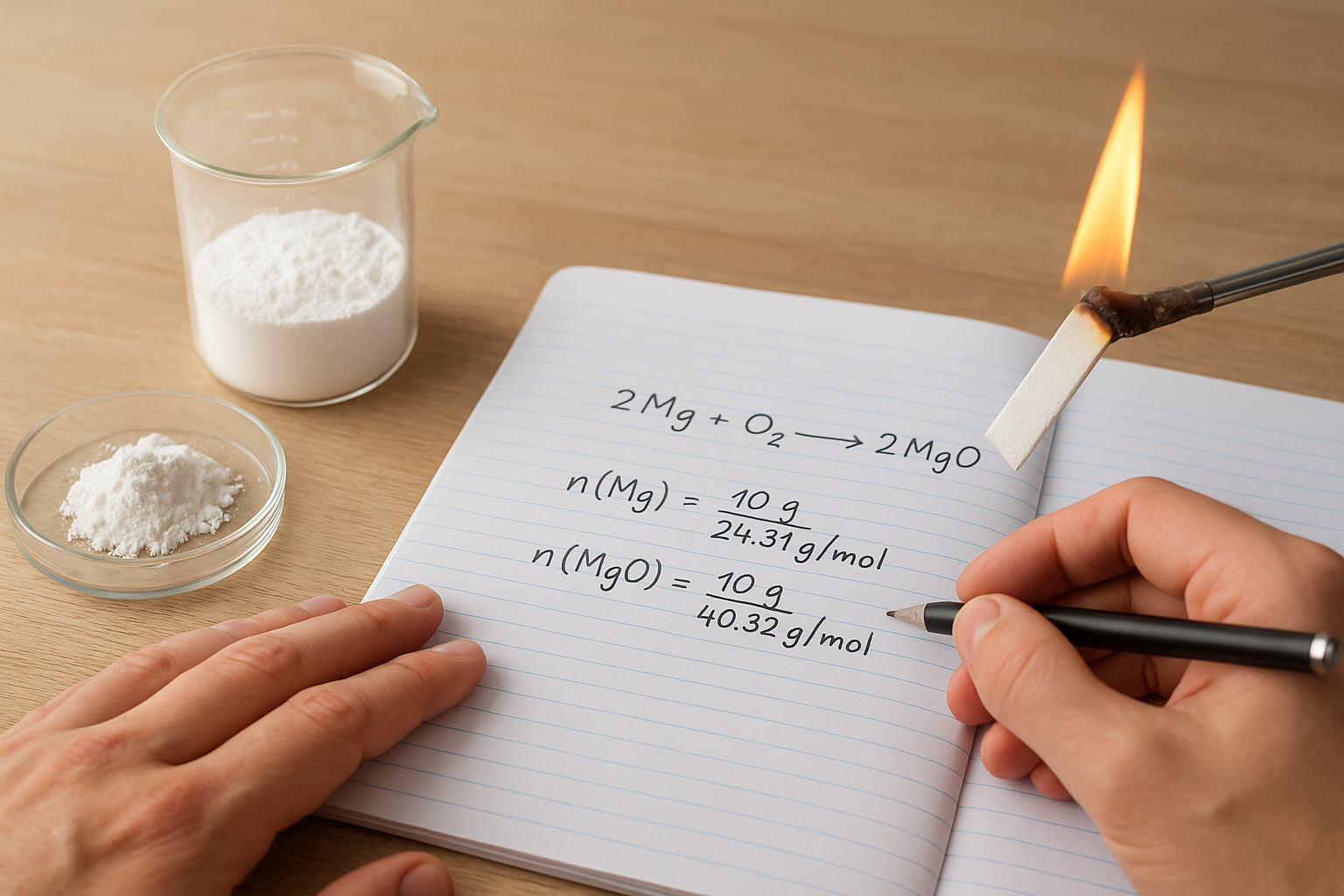Sztöchiometriai számítások: Mennyi magnézium-oxid keletkezik az égéskor?
A sztöchiometriai számítások a kémia egyik legizgalmasabb és leghasznosabb területét jelentik. Lényege, hogy kémiai reakciók során meghatározzuk, milyen mennyiségekben reagálnak egymással az anyagok, illetve milyen mennyiségű termék keletkezik. Ez a tudás nélkülözhetetlen a laboratóriumi gyakorlatban, az iparban, vagy akár a mindennapi életben, például háztartási vegyszerek helyes adagolásánál.
A magnézium égése során keletkező magnézium-oxid mennyiségének kiszámítása kiváló példája a sztöchiometriai műveleteknek. Ez a folyamat nemcsak azt mutatja meg, hogyan lehet egy egyszerű reakciót matematikailag leírni, hanem azt is, hogy a való életben milyen tényezők befolyásolják a kapott eredményeket. Ezen számítások ismerete segít pontosabban tervezni, kísérletezni, és hatékonyabban felhasználni az erőforrásokat.
A sztöchiometria az alapja a kvantitatív kémiai elemzéseknek, legyen szó ipari vegyiparról, környezetvédelmi mérésekről vagy akár az iskolai laboratóriumokról. Akár kezdőként, akár haladóként használod, a sztöchiometriai számítások alkalmazása lehetővé teszi, hogy pontos képet kapj egy adott reakció végtermékéről, azaz jelen esetben a magnézium-oxid tömegéről.
Tartalomjegyzék
- Bevezetés a sztöchiometriai számítások világába
- Magnézium égése: kémiai reakció bemutatása
- A magnézium-oxid keletkezésének folyamata
- Kémiai egyenlet felírása és rendezése
- Anyagmennyiség fogalma és szerepe a sztöchiometriában
- Relatív atomtömeg és moláris tömeg meghatározása
- Kiindulási anyag tömegének pontos mérése
- Molok számítása a kiindulási magnéziumból
- Aránypárok a reakcióban: magnézium és oxigén
- Magnézium-oxid elméleti tömegének kiszámítása
- Lehetséges eltérések a gyakorlati eredményektől
- Összegzés: a sztöchiometriai számítások jelentősége
- GYIK (Gyakran Ismételt Kérdések)
Bevezetés a sztöchiometriai számítások világába
A sztöchiometria a kémia azon ága, amely a kémiai reakciók során bekövetkező anyagátalakulások mennyiségi viszonyait vizsgálja. A szó a görög "stoicheion" (elem) és "metron" (mérték) szavakból származik, utalva arra, hogy az anyagok átváltozását pontos arányok jellemzik. A sztöchiometriai számítások során meghatározzuk, hogy adott mennyiségű kiindulási anyagból hány mól vagy gramm termék képződik.
Ez a tudományterület elengedhetetlen a kémia tanulásához és gyakorlati alkalmazásához. Segítségével tervezhető egy laboratóriumi vagy ipari folyamat, optimalizálhatóak a nyersanyag-felhasználások, és minimalizálható a hulladék. A sztöchiometriai számítások lehetővé teszik, hogy egy reakciót pontosan, gazdaságosan és biztonságosan végezzünk el.
A sztöchiometria az élet minden területén jelen van. Legyen szó gyógyszergyártásról, élelmiszeriparról, környezetvédelmi mérésekről vagy akár a mindennapi sütés-főzésről, mindenhol fontos tudni, hogy milyen arányban keverjük az anyagokat a kívánt eredmény eléréséhez. Ezért a sztöchiometriai számítások ismerete minden kémiaszakos hallgató és érdeklődő számára alapvető.
Magnézium égése: kémiai reakció bemutatása
A magnézium égése az egyik legismertebb és leglátványosabb kémiai reakció, amelyet gyakran bemutatnak az iskolai kísérletek során. Amikor a magnéziumot meggyújtjuk, az erőteljes, vakító fehér fénnyel ég, miközben a levegő oxigénjével reagál. A folyamat során magnézium-oxid (MgO) keletkezik, amely fehér, por alakú szilárd anyagként jelenik meg.
A reakció exoterm jellegű, vagyis hőt szabadít fel. Ez nemcsak a látványos fényjelenség miatt érdekes, hanem azért is, mert a magnézium égése jól szemlélteti, hogyan használhatók fel a kémiai energiák gyakorlati célokra, például világításra vagy hőtermelésre. A magnézium égése során lejátszódó folyamatok pontos megértése fontos a tűzvédelem, a fémipar és az oktatás szempontjából is.
A magnézium-oxid keletkezésének folyamata
A magnézium-oxid keletkezése egyszerű, de tanulságos kémiai folyamat. A magnézium (Mg) atomjai reakcióba lépnek az oxigén (O₂) molekulákkal, melyek a levegőben találhatók. A reakció során minden egyes magnéziumatom egy oxigénatommal egyesül, hogy magnézium-oxidot (MgO) hozzon létre.
Ez a folyamat jól mutatja a kémiai elegyedési arányokat és a reakciók során érvényesülő tömegmegmaradás törvényét. Ha pontosan mérjük a kiindulási magnézium tömegét, akkor meghatározhatjuk, hogy elméletileg mennyi magnézium-oxid képződik, ha az összes magnézium reakcióba lép az oxigénnel. Ez a számítás a sztöchiometria egyik klasszikus példája.
Kémiai egyenlet felírása és rendezése
A kémiai reakcióknál elengedhetetlen a helyes egyenlet felírása és rendezése. Ez biztosítja, hogy a számításaink pontosak legyenek, hiszen a sztöchiometriai arányokat ebből olvassuk le. A magnézium égésének egyszerűsített, rendezett egyenlete:
Mg + ½ O₂ → MgO
Ez azt jelenti, hogy egy mól magnézium reagál fél mól oxigénnel (azaz egy atom oxigénnel) és egy mól magnézium-oxid keletkezik. A mérlegelés során mindig ügyelni kell arra, hogy az atomok száma mindkét oldalon megegyezzen. Ez a tömegmegmaradás törvényének alapja.
A rendezett kémiai egyenlet segít abban, hogy megállapítsuk, hány mól reaktánsra (magnézium és oxigén) és hány mól termékre (magnézium-oxid) számíthatunk. Ez a kiindulópontja minden további sztöchiometriai számításnak.
Anyagmennyiség fogalma és szerepe a sztöchiometriában
Az anyagmennyiség (jele: n) a kémia egyik kulcsfogalma. Ez mutatja meg, hogy adott anyagból hány "darab" részecskénk (atom, molekula, ion) van, méghozzá a standard SI-mértékegység, a mól segítségével. Egy mól pontosan 6,022 × 10²³ darab részecskét jelent (ez az Avogadro-szám).
A sztöchiometriában az anyagmennyiség azért fontos, mert a kémiai reakciók mólokban zajlanak. Ha tudjuk, hogy mennyi mól magnézium áll rendelkezésre, kiszámíthatjuk, hogy mennyi mól magnézium-oxid kelhetkezik. Ez az első lépés a tömeg, a térfogat vagy akár a részecskeszám meghatározásához.
Relatív atomtömeg és moláris tömeg meghatározása
A relatív atomtömeg (jele: Ar) egy adott elem atomjának tömegét mutatja meg a szén-12 izotóp tömegéhez viszonyítva. A magnézium relatív atomtömege például 24, míg az oxigéné 16. Ezek az értékek megtalálhatók a periódusos rendszerben, és elengedhetetlenek a sztöchiometriai számításokhoz.
A moláris tömeg (jele: M) egy mól anyag tömegét adja meg, gramm/mol egységben. Például a magnézium moláris tömege 24 g/mol, az oxigéné 16 g/mol, a magnézium-oxidé pedig 40 g/mol (24 + 16). Ezek az adatok segítenek átszámolni az anyagmennyiséget tömegre, vagy fordítva, így könnyen összevethetjük a mért adatokat az elméleti eredményekkel.
Kiindulási anyag tömegének pontos mérése
A sztöchiometriai számítások alapja minden esetben a kiindulási anyag pontos tömege. Ha például azt szeretnénk tudni, hogy adott tömegű magnéziumból mennyi magnézium-oxid keletkezik, először le kell mérnünk a magnézium tömegét egy pontos mérlegen.
A mérésnél fontos, hogy a mintánk tiszta legyen, és ne legyen benne idegen anyag vagy szennyeződés. Egy tipikus laboratóriumi mérleg 0,01 g pontossággal mér. Amint megvan az adat, máris kezdhetjük a számítást – a tömeg alapján meghatározhatjuk a kiindulási mólok számát.
Molok számítása a kiindulási magnéziumból
Most, hogy ismert a magnézium tömege, kiszámíthatjuk, hány mól magnézium áll rendelkezésre a reakcióhoz. A számítás a következőképpen történik: a magnézium tömegét elosztjuk a moláris tömeggel.
Ha például 2,4 g magnéziumot használunk, az anyagmennyiség:
n = m ÷ M
Ahol
n: anyagmennyiség (mol)
m: tömeg (g)
M: moláris tömeg (g/mol)
Ez az első lépés a magnézium-oxid mennyiségének meghatározásához, hiszen a kémiai egyenletből következően a molok aránya adja meg, mennyi termék keletkezik.
Aránypárok a reakcióban: magnézium és oxigén
A sztöchiometriai arányok a kémiai egyenletből olvashatók ki. A magnézium égésének rendezett egyenlete szerint:
Mg + ½ O₂ → MgO
Ez azt jelenti, hogy egy mól magnézium pontosan egy mól magnézium-oxidot eredményez. Az oxigén mennyiségét is meghatározhatjuk az arányok alapján: minden egyes mól magnéziumhoz fél mól oxigén szükséges.
Ezek az arányok lehetővé teszik, hogy bármilyen kiindulási tömegre kiszámoljuk a magnézium-oxid várható tömegét. Ha a magnézium a limitáló reagens, akkor abból indulunk ki, de ha az oxigén mennyisége lenne korlátozott, azt is figyelembe kellene venni.
Magnézium-oxid elméleti tömegének kiszámítása
A következő lépésben meghatározzuk, hogy az adott mennyiségű magnéziumból mennyi magnézium-oxid keletkezik. Ehhez először a magnézium anyagmennyiségét számítjuk ki, majd a kémiai egyenlet arányai alapján megállapítjuk, mennyi mól magnézium-oxid képződik.
Ezután a magnézium-oxid tömegét úgy kapjuk meg, hogy a keletkező mólokat megszorozzuk a MgO moláris tömegével:
m(MgO) = n(MgO) × M(MgO)
Így megtudhatjuk, hogy adott magnézium-mennyiségből mennyi magnézium-oxidot várhatunk elméletileg, ha a reakció teljesen végbemegy.
Táblázat: Magnézium-oxid keletkezésének lépései
| Lépés | Művelet | Példa (2,4 g Mg esetén) |
|---|---|---|
| 1. mérés | m(Mg) mérleggel | 2,4 g |
| 2. anyagmennyiség | n = m ÷ M | 2,4 g ÷ 24 g/mol = 0,1 mol |
| 3. arány | n(MgO) = n(Mg) | 0,1 mol |
| 4. tömeg | m = n × M | 0,1 mol × 40 g/mol = 4,0 g |
Táblázat: A folyamat előnyei és hátrányai
| Előnyök | Hátrányok |
|---|---|
| Pontos eredmény | Mérési hibák lehetségesek |
| Tervezhető reakciók | Számolási hibák előfordulnak |
| Hulladék minimalizálása | Nem veszi figyelembe a veszteségeket |
Táblázat: Gyakran használt SI prefixumok tömegre
| Prefixum | Jelentés | Példa |
|---|---|---|
| milli | 0,001 | 1 mg = 0,001 g |
| kilo | 1 000 | 1 kg = 1 000 g |
| mikro | 0,000001 | 1 μg = 0,000001 g |
Lehetséges eltérések a gyakorlati eredményektől
A valóságban a mért magnézium-oxid tömege gyakran eltér az elméletileg számított értéktől. Ennek számos oka lehet, például:
- A magnézium nem ég teljesen el – részben oxidáció nélkül marad.
- Néhány magnézium-oxid részecske elszáll a reakció során.
- Szennyeződések jelenléte mind a kiindulási, mind a keletkező anyagban.
Ezek a tényezők mind befolyásolják a reakció hozamát, azaz azt, hogy az elméleti maximumhoz képest ténylegesen mekkora tömegű magnézium-oxid képződik. A laboratóriumi gyakorlatban ezért fontos a kísérleteket többször ismételni, a tömegméréseket pontosan végezni, és minden lehetséges veszteségre figyelni.
Összegzés: a sztöchiometriai számítások jelentősége
Ahogy látható, a sztöchiometriai számítások nélkülözhetetlenek minden kémiai folyamat megértéséhez és irányításához. Akár a laboratóriumban dolgozol, akár otthon végzel egyszerű kísérleteket, a helyes számítások segítenek a nyersanyagok hatékony felhasználásában, a reakciók hozamának növelésében, és a veszteségek minimalizálásában.
A magnézium égése és a magnézium-oxid keletkezése kiváló példája a sztöchiometria gyakorlati alkalmazásának. Ha megérted a folyamat lépéseit, a kémiai egyenletek jelentését és az anyagmennyiségek kiszámítását, magabiztosan kezelheted a hasonló számításokat bármilyen más kémiai reakció esetén is.
GYIK – Gyakran Ismételt Kérdések
-
Mit jelent a sztöchiometria?
A kémiai reakciók mennyiségi viszonyainak vizsgálata, amely segít meghatározni, hogy adott mennyiségű kiindulási anyagból mennyi termék keletkezik. -
Miért fontos a kémiai egyenlet rendezése?
Az atomok és tömegek megmaradásának elve miatt, így helyesek lesznek a számítások. -
Mi az a mól?
Az anyagmennyiség SI-egysége, amely 6,022 × 10²³ részecskét jelent. -
Mi a moláris tömeg?
Egy mól anyag tömege grammokban, a periódusos rendszerből olvasható ki. -
Mitől függ a keletkező magnézium-oxid tömege?
A kiindulási magnézium tömegétől és tisztaságától, valamint attól, hogy mennyire teljes a reakció. -
Mit jelent a limitáló reagens?
Az az anyag, amelyből kevesebb áll rendelkezésre a szükségesnél, így az szabja meg a termék mennyiségét. -
Miért lehet alacsonyabb a gyakorlati hozam az elméletinél?
Mert mérési hibák, anyagveszteség vagy szennyeződések léphetnek fel a reakció során. -
Hogyan számolom ki a magnézium mólok számát?
A tömegét elosztod a moláris tömegével. -
Miért kell ismerni a relatív atomtömegeket?
Mert ezekből számolható ki a moláris tömeg, amely minden további átszámításhoz kell. -
Hol alkalmazható még a sztöchiometria?
Az iparban, gyógyszergyártásban, környezetvédelemben, oktatásban, bármilyen kémiai folyamatban.